
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
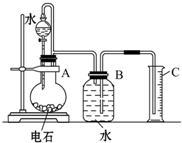 ijͬѧÉčĽĆÁËČçÍĽËůĘľµÄʵŃé×°ÖĂŔ´´ÖÂԵزⶨµçĘŻÖĐĚĽ»Ż¸ĆµÄÖĘÁż·ÖĘýŁ®
ijͬѧÉčĽĆÁËČçÍĽËůĘľµÄʵŃé×°ÖĂŔ´´ÖÂԵزⶨµçĘŻÖĐĚĽ»Ż¸ĆµÄÖĘÁż·ÖĘýŁ®| 0.29V |
| W |
| 0.29V |
| W |
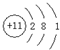

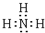
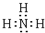

 ČýÖÖ»ůÍĹŁ¬ÎŢ»·×´˝áąąŁ¬ČýÖÖ»ůÍŵÄĘýÄżąŘϵΪn3=
ČýÖÖ»ůÍĹŁ¬ÎŢ»·×´˝áąąŁ¬ČýÖÖ»ůÍŵÄĘýÄżąŘϵΪn3=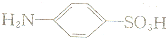 Ł©·ŰÄ©Ł¬˝áąűČçĎÂŁşŁş
Ł©·ŰÄ©Ł¬˝áąűČçĎÂŁşŁş| É«˝×ĐňşĹ | 1 | 2 | 3 | 4 | 5 | 6 |
| ĽÓČëČÜŇşBµÄĚĺ»ýŁ¨mL | 0.0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
| ·´Ó¦şóČÜŇşŃŐÉ« | ÓÉÎŢÉ«±äÎŞÓÉÇłµ˝ÉîµÄÓŁĚŇşěÉ« | |||||

Ň»ˇ˘1.D 2.B 3.A 4.B 5.BD 6.B 7.BC 8.B 9.B?
¶ţˇ˘10.˘Ů2 2 ?
˘ÚCH
11.2NaClŁ«2H2O 2NaOHŁ«H2ˇüŁ«Cl2ˇü?
2NaOHŁ«H2ˇüŁ«Cl2ˇü?
H2Ł«Cl2 2HCl?
2HCl?
CaCO3 CaOŁ«CO2ˇü?
CaOŁ«CO2ˇü?
CŁáOŁ« CŁáC2Ł«COˇü?
CŁáC2Ł«COˇü?
CaC2Ł«2H2O===CaŁ¨OHŁ©2Ł«C2H2ˇü?
 |
2CHˇÔCH CH2==CH¨DCˇÔCH
CH2==CH¨DCˇÔCHŁ«HCl CH2==CH¨DCCl==CH2
CH2==CH¨DCCl==CH2

12.(1)CaC2µÄÖĘÁż·ÖĘýÎŞ86%?
(2)Ęą˛â¶¨˝áąűĆ«´ó?
13.Ł¨1Ł©BŁ¨CH3Ł©3+2HBr BŁ¨CH3Ł©Br2+2CH4Ł»
BŁ¨CH3Ł©Br2+2CH4Ł»
Ł¨2Ł©4ˇĂ1
14.ŇŔľÝ¸÷ŔŕÁ´ĚţµÄČĽÉŐͨʽŁ¬˝áşĎÉúłÉµÄCO2ˇ˘H2OµÄĚĺ»ýŁ¬żÉ·ÖŇÔĎÂÇéżöĚÖÂŰŁş?
Ł¨1Ł©ČôÎŞÍéĚţŁ¬ÓĐ
Ă÷ĎԵأ¬ÓĐ ˇÜxŁĽ1Ł¬n=
ˇÜxŁĽ1Ł¬n=
Ł¨2Ł©ČôÎŞĎ©ĚţŁ¬ÓĐ Ł¬Ôňx=1Ł¬nˇÝ2ˇŁ
Ł¬Ôňx=1Ł¬nˇÝ2ˇŁ
Ł¨3Ł©ČôΪȲĚţŁ¬
Ôň1ŁĽxˇÜ2Ł¬n=
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com