
题目列表(包括答案和解析)
| A、3.4mol?L-1 | B、0.2mol?L-1 | C、1.8mol?L-1 | D、3.6 mol?L-1 |
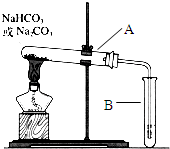 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.
某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.| 组 别 | 1 | 2 | 3 |
| 固体质量/g | 3.80 | 6.20 | 7.20 |
| 气体质量/g | 1.76 | 2.64 | 2.64 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com