
题目列表(包括答案和解析)
(1)甲烷、乙烯、苯三种有机物中具有下列性质的是
①在催化剂作用下能与纯溴反应,不能使酸性高锰酸钾溶液褪色的是 ;
②见光能跟氯气反应,不能使酸性高锰酸钾溶液褪色的是 ;
③在催化剂作用下加氢生成乙烷,加水生成酒精的是 。
(2)如图是两种有机物的球棍模型,○代表H原子,●代表C原子,请回答下列问题: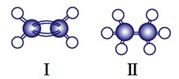
①写出Ⅰ、Ⅱ的化学式 、
②说出Ⅰ、Ⅱ在结构上的两点差异 ,
(1)甲烷、乙烯、苯三种有机物中具有下列性质的是
①在催化剂作用下能与纯溴反应,不能使酸性高锰酸钾溶液褪色的是 ;
②见光能跟氯气反应,不能使酸性高锰酸钾溶液褪色的是 ;
③在催化剂作用下加氢生成乙烷,加水生成酒精的是 。
(2)如图是两种有机物的球棍模型,○代表H原子,●代表C原子,请回答下列问题:
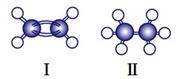
①写出Ⅰ、Ⅱ的化学式 、
②说出Ⅰ、Ⅱ在结构上的两点差异 ,
(1)单质钙能与冷水反应,其反应的化学方程式:____________________;此反应远不如钠和水反应剧烈,其原因可能是___________________________________________________。
(2)将钙投入盐酸中,能否发生反应____________(填“能”或“不能”),如果能发生反应,写出反应的化学方程式:____________________________。
(3)在金属活动性顺序表中,钙排在钠的前面。将钙投入钠盐溶液中,可能发生的现象是____________,所发生反应的化学方程式:_____________________________________。
(4)自然界里____________(填“存在”或“不存在”)游离态的钙,就你所知,自然界里存在最大量的化合态钙是___________________________。
(5)现在市场上常见的一种保健药品,名为“巨能钙”,请你推测一下,此药品中的钙元素是____________(填“游离”或“化合”)态,理由是________________________________。

 +RX
+RX| 催化剂 |
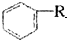 +HX(R.是烃基,X为卤原子)
+HX(R.是烃基,X为卤原子) A、B、D、E是短周期中构成蛋白质的重要元素,其性质见下表.Fe、Co元素的常见化合价为+2、+3,能形成各种有色配离子.
A、B、D、E是短周期中构成蛋白质的重要元素,其性质见下表.Fe、Co元素的常见化合价为+2、+3,能形成各种有色配离子.| A | B | D | E | |
| 化合价 | -4 | -2 | -3 | -2 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com