
题目列表(包括答案和解析)


| ||
| ||
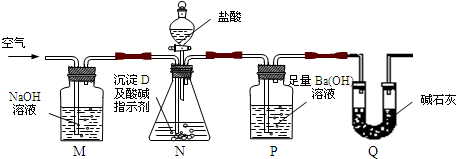
| 实验步骤 | 预期现象和结论 | 步骤1:取适量牙膏样品加水充分搅拌、过滤,得滤液A和沉淀B. | / | 步骤2:取适量滤液A于试管中, |
有 |
步骤3:取适量沉淀B于试管中,加入过量 |
/ | 步骤4:往所得滤液中通入过量二氧化碳. | 产生成白色沉淀, |
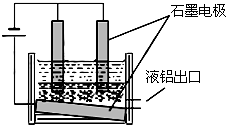 [化学-化学与技术]
[化学-化学与技术]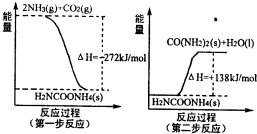
| 温度/ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
2- 3 |
- 3 |
2- 3 |
- 3 |
- 3 |
2- 3 |
2- 3 |
- 3 |
一、选择题:(共44分)
1.D 2.A 3.D 4.B 5.A 6.D 7.C 8.C 9.A 10.C 11.B
12.D 13.B 14.A 15.C 16.C 17.A 18.B 19.A 20.C 21.B 22.B
二. 填空题(本题共4小题,共48分)
23.(8分,每空2分) K2Cr2O7 是氧化剂, HCl 是还原剂,
Cl 元素被氧化, Cr 元素被还原,
Cl2 是氧化产物, CrCl3 是还原产物。
 |
K2Cr2O7 +14HCl=2KCl+2CrCl3+3Cl2↑+7H2O(标出电子转移方向和数目)
24.(14分,每空2分)
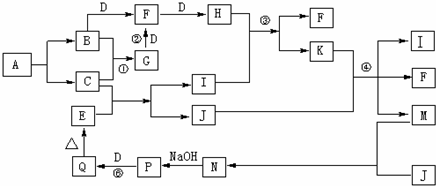
(1)化学式:A Ba(OH)2 B H2SO
(2)反应①、②、⑤的离子方程式
① SO42-+ 2H++ ba2++2oh-= baSo4↓+2H2O
② CO32-+ 2H+ = CO2 ↑+ H2O
⑤ Mg2+ + 2oh- = Mg(OH)2↓
25.(14分,每空2分)三种离子: OH- 、 K+ 、 Cl- 。
铁粉 , 银 ,
Ag+ 、 Fe3+ , NO3- 、 K+ 。
26.(12分,每空2分) (1)
(2)500mL容量瓶、烧杯、玻璃棒、胶头滴管。
(3)A、_无影响____ B、____偏高_
C、__偏低____ D、 _偏低_ 。
三. 计算题(本题共1小题,共8分)
27.(1)氧化剂是 MnO2 (2分 )
(2) ①168mL(3分 )
②1mol (3分 )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com