
题目列表(包括答案和解析)
海波(Na2S2O3·5H2O)可用作脱氯剂、定影剂、解毒剂.硫粉和亚硫酸纳溶液煮沸可制得Na2S2O3·5H2O;Na2S2O3·5H2O的部分性质见下表:
实验室制备海波过程如下:

(1)实验开始时,加入1 mL C2H5OH的目的是________
(2)滤液A中除有Na2S2O3和少量Na2SO3外,最可能存在的无机化合物杂质是________,如果滤液中该杂质的含量不很低,其检测的方法是________
(3)过滤操作所用的玻璃仪器有________,过滤后发现滤渣B中有少量淡黄色物质.为除去淡黄色物质,洗涤滤渣B的操作过程是__________________
(4)烘干滤渣B时应注意什么问题________,原因是__________________
海波 (Na2S2O3•5H2O) 可用作脱氯剂、定影剂、解毒剂。硫粉和亚硫酸纳溶液煮沸可制得 Na2S2O3•5H2O;Na2S2O3•5H2O的部分性质见下表:
| 物理性质 | 易溶于水,不溶于乙醇;熔点 48.2℃;在潮湿的空气中易潮解 |
| 化学性质 | 43℃以上的空气中易风化;遇酸易分解 (S2O32+2H+=S↓+SO2↑+H2O ) |
实验室制备海波过程如下:
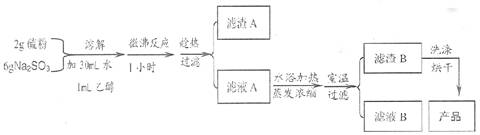
(1)实验开始时,加入1 mL C2H5OH 的目的是
(2)滤液 A 中除有Na2S2O3和少量 Na2SO3 外,最可能存在的无机化合物杂质是
, 如果滤液中该杂质的含量不很低,其检测的方法是
(3)过滤操作所用的玻璃仪器有 , 过滤后发现滤渣 B 中有少量淡黄色物质。为除去淡黄色物质,洗涤滤渣 B 的操作过程是
(4)烘干滤渣 B 时应注意什么问题 ,原因是
(11分 )海波 (Na2S2O3•5H2O) 可用作脱氯剂、定影剂、解毒剂。硫粉和亚硫酸纳溶液煮沸可制得 Na2S2O3•5H2O;Na2S2O3•5H2O的部分性质见下表:
| 物理性质 | 易溶于水,不溶于乙醇;熔点 48.2℃;在潮湿的空气中易潮解 |
| 化学性质 | 43℃以上的空气中易风化;遇酸易分解 (S2O32―+2H+=S↓+SO2↑+H2O ) |
实验室制备海波过程如下:

(1)实验开始时,加入1 mL C2H5OH 的目的是
(2)滤液 A 中除有Na2S2O3和少量Na2SO3 外,最可能存在的无机化合物杂质是 , 如果滤液中该杂质的含量不很低,其检测的方法是
(3)过滤操作所用的玻璃仪器有 , 过滤后发现滤渣 B 中有少量淡黄色物质。为除去淡黄色物质,洗涤滤渣 B 的操作过程是
(4)烘干滤渣 B 时应注意什么问题 ,原因是
(11分 )海波 (Na2S2O3•5H2O) 可用作脱氯剂、定影剂、解毒剂。硫粉和亚硫酸纳溶液煮沸可制得 Na2S2O3•5H2O;Na2S2O3•5H2O的部分性质见下表:
|
物理性质 |
易溶于水,不溶于乙醇;熔点 48.2℃;在潮湿的空气中易潮解 |
|
化学性质 |
43℃以上的空气中易风化;遇酸易分解 (S2O32―+2H+=S↓+SO2↑+H2O ) |
实验室制备海波过程如下:

(1)实验开始时,加入1 mL C2H5OH 的目的是
(2)滤液 A 中除有Na2S2O3和少量 Na2SO3 外,最可能存在的无机化合物杂质是 , 如果滤液中该杂质的含量不很低,其检测的方法是
(3)过滤操作所用的玻璃仪器有 , 过滤后发现滤渣 B 中有少量淡黄色物质。为除去淡黄色物质,洗涤滤渣 B 的操作过程是
(4)烘干滤渣 B 时应注意什么问题 ,原因是
实验室制备乙酸乙酯的反应和实验装置如下:
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
投料 1 : 1 产率 65%
1 : 10 97%
(在120 ℃下测定)
已知:相关物理性质(常温常压)
| | 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | ~117 | 溶 |
| 乙酸乙酯 | 0.902 | ?84 | ~76.5 | 不溶 |




一、选择题(1~10小题,每小题3分,共30分;11~20小题最多两个答案,每小题4分,答对一个得2分,答对两个得4分,但只要答错一个得0分)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
A
B
D
A
C
D
A
D
题号
11
12
13
14
15
16
17
18
19
20
答案
AD
A
D
D
BD
C
BC
AD
B
A
三、(共30分)
21、(7分)(1)CH3-O-CH2-OH CH2OH-CH2OH (各1分,共2分)
(2)(各1分,共2分。预期生成H2的体积与对应X的结构简式都对才得1分,只答对一部分不得分;体积没有单位合并扣1分,单位用毫升表示不扣分)
实验原理
预期生成H2的体积(标况)
对应X的结构简式
取
1.
CH3-O-CH2-OH
2.
CH2OH-CH2OH
(3)(3分,装置可参考图示1或2,其它如附图的合理答案也得分。进气管和出水管的顺序颠倒扣1分)
 |
|||||
 |
|||||
 |
|||||
图示1 图示2
 |
|||
 |
|||

22、(12分)(1)11.76~11.78均得分 (1分) (2)Na2CO3 和NaHCO3 (1分)因为第一滴定终点所用体积小于第二滴定终点所用体积或V1<(V2-V1)或计算说明 (2分)
(3)以防滴定过快使Na2CO3直接生成H2CO3 (2分)
(4)碱样的总碱量为:
n(Na2O)= [(25.02mL +24.98 mL)/2]×10
(5)直接以溴甲酚绿-二甲基黄或甲基橙为指示剂滴定至终点 (3分)
23、(11分)(1)便于硫被水浸润 (2分)
(2)Na2SO4(1分) 取少量溶液,加稀盐酸酸化后,过滤,再加BaCl2溶液 (2分)
(3)玻璃棒、漏斗、烧杯 (2分);用乙醇或CS2浸没滤渣,等自然流下后,重复几次(2分)。(用水洗涤不得分)
(4)温度应低于
四、(共30分)
24.(11分)(1)NaOH、NaAl(OH)4(NaAlO2)、Na2SiO3 [或氢氧化钠、铝酸钠(偏铝酸钠)、硅酸钠](1分)
(2)CO2+2OH-==HCO3-+2H2O (1分) ,CO2+3H2O+2AlO2-==2Al(OH)3↓+2H2O-+CO32- (1分)
(3) bac (2分) ;
(4)2H2O+2e-→2OH-+H2↑(2分) ;Al(OH)3 +OH-=Al(OH)4- 或Al(OH)3 +OH-=AlO2-+2H2O (2分)
 (5)(2分)
(5)(2分)
25 (8分)
(1)(3分)
V正 < V逆(1分)
0.40(2分)
(2)25%(1分);不变(1分);1:a(1分); (3)-78.7 (2分)
26(11分)(1) (2分)
(2分)
(2)①NH3 或NH4+ (1分);其规律是:硝酸的浓度越大,其还原产物中氮元素化合价越高。(2分)
(其它合理答案均给分。如硝酸的浓度越大,气体生成物中二氧化氮的含量越高;或者,只在硝酸浓度较低时,产物中才会出现氮气。等等)
②B、C、D (对一个或两个给一分,全对2分,但只要出现A、E便不给分) (2分)
③硝酸易挥发,且不稳定,见光易分解,故不易操作;生成物对环境污染严重 (2分)
(3)A.B.D.(2分)(对一个或两个给一分,全对2分,但只要出现C便不给分)
五、(共10分)
27. (共10分) (1)BCD;(共2分,答对两个给1分全对给2分,错选A倒扣1分,答ABCD为0分)
(2)能与羧酸发生酯化反应(或其它合理的答案均可);(2分)
(3)CH3COOH;(2分,写结构式不给分)
(4)AC;(2分,选对一个给一分,错选一个倒扣一分,扣完本小题分为止)
(5)CH2=CH2 + Br2 → CH2Br―CH2Br;(2分,有机物写分子式不给分、写结构式给分,“→”写“=”不给分)
六、选做题(共10分)
28. (共10分)
 |
(1) (2分),取代反应(或酯化反应);(1分)
 |
(2)
(2分,有机物写分子式不给分、写结构式给分,
“→”写“=”扣1分,反应条件错写或漏写扣1分)
(3)b、c、d;(2分,选对两个给1分,选对三个给2分,错选为0分)
 (4)(3分,路线有误或不全者不给分,条件不全或有误者扣一分,其它合理答案酌情给分)
(4)(3分,路线有误或不全者不给分,条件不全或有误者扣一分,其它合理答案酌情给分)
 |
或者
29.(共10分)
(1)LaNi5 + 3H2  LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
(2)CE (2分,每选对一个给一分,每错选一个倒扣一分,扣完本小题分为止)
(3)①[Ar]3d7;或 (2分,写成3d7不给分)
(2分,写成3d7不给分)
②2NiO(OH) + 6HCl(浓)=2NiCl2+Cl2↑+4H2O;(2分,未配平不给分,氯气未写气体符号扣一分)
(4)A和B(或A和C、A和D、B和E、C和E、D和E任一组均可);(2分,若同组中出现同种物质则不给分,例如AE、BC……等)
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com