
题目列表(包括答案和解析)
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.

| ||
| △ |
| ||
| △ |
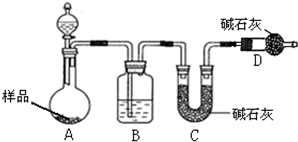 为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:
为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:(一)制取氨气
(1)写出实验室制取氨气的化学方程式:________________。
(2)有一同学模仿排饱和食盐水收集氯气的方法用排饱和氯化铵溶液的方法收集氨气。但另一同学认为他不能达到目的,理由是_____________________________________________。
(二)该小组某同学设计如下图装置(夹持及尾气处理装置未画出),探究氨气的还原性:
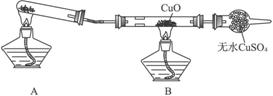
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是__________________。
(2)利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为_________________。
(三)问题讨论
有同学认为NH3与CuO反应生成的红色物质中可能含有Cu2O,已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+![]() Cu+Cu2+)。请设计简单实验检验该红色物质中是否含有Cu2O:____________。
Cu+Cu2+)。请设计简单实验检验该红色物质中是否含有Cu2O:____________。
【10分】某些同学在学习了氨的性质时探究讨论:既然氨气具有还原性,能否像H2那样还原CuO呢?
(一)制取氨气
(1)写出实验室制取氨气的化学方程式:________________。
(2)有一同学模仿排饱和食盐水收集氯气的方法用排饱和氯化铵溶液的方法收集氨气。但另一同学认为他不能达到目的,理由是_____________________________________________。
(二)该小组某同学设计如下图装置(夹持及尾气处理装置未画出),探究氨气的还原性:
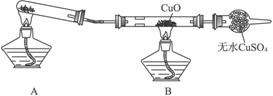
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是__________________。
(2)利用改进后的装置进行实验,CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。氨气与CuO反应的化学方程式为_________________。
(三)问题讨论
有同学认为NH3与CuO反应生成的红色物质中可能含有Cu2O,已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+![]() Cu+Cu2+)。请设计简单实验检验该红色物质中是否含有Cu2O:____________。
Cu+Cu2+)。请设计简单实验检验该红色物质中是否含有Cu2O:____________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
D
D
A
B
D
D
C
D
B
B
B
C
C
A
C
C
B
A
19.(8分)( 1 ) B D ( 2 分)
(2)一定有 NO3-、Al3+、SO42-(2分); 一定无 Fe3+、Ba2+、HCO3-(2分)
(3) Al3+ + 3 NH3?H2O = Al(OH)3↓+3NH4+ (2分)
 20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)
20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)
|