
题目列表(包括答案和解析)
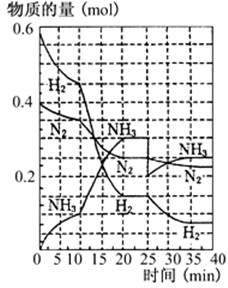 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )| A、反应开始到第一次平衡时,N2的平均反应速率为0.005mol/(L?min) | B、从曲线可以看出,反应进行到10min至20min时可能是使用了催化剂 | C、从曲线可以看出,反应进行至25min时,增加了0.1mol氨气 | D、在25min平衡正向移动但达到新平衡后NH3的体积分数比原平衡小 |
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N22NH3 △H<0。反应过程中H2、N2和NH3物质的量变化如右图所示,据图判断下列叙述不正确的是

A.反应开始到第一次平衡时,N2的平均反应速率为0.0625 mol·(L·min)-1 ,H2的转化率为75%
B.反应达到第一次平衡时,反应的平衡常数表达式可写作:K=c2(NH3)/[ c3(H2) ·c(N2)]=(0.15 mol·L-1) 2/[ (0.075 mol·L-1) 3 ·(0.125 mol·L-1)]
C.从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂
D.从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动
500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是
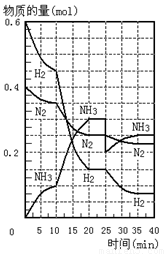
A.反应开始到第一次平衡时,N2的平均反应速率为0.005mol/(L·min)
B.从曲线变化可以看出,反应进行到10min至20min钟时可能是使用了催化剂
C.从曲线变化可以看出,反应进行至25min钟时,分离出0.2mol的氨气
D.在25min钟时平衡正向移动但达到新平衡后 NH3的体积分数比原平衡小
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应反应过程中H2、N2和NH3物质的量变化如下图所示,下列说法正确的是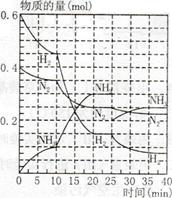
| A.反应开始到第一次平衡时,N2的平均反应速率为0.005 mol/(L·min) |
| B.从曲线可以看出,反应进行到10min至20min时可能是使用了催化剂 |
| C.从曲线可以看出,反应进行至25min时,增加了0.1mol氨气 |
| D.在25min平衡正向移动但达到新平衡后NH3的体积分数比原平衡小 |
500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中
H2、N2和NH3物质的量变化如图所示,根据题意完成下列各题:
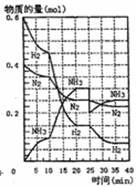
(1)反应达到平衡时,平衡常数表达式K= 此时增加N2的量,平衡常数将 (填“增大”“减小”或“不变”)
(2)500℃、20Mpa时,反应处于平衡状态的时间 。
(3)反应开始到第一次平衡时,N2的平均反应速率为 。
(4)据图判断,反应进行到10min至20min时曲线发生变化的原因是: 反应进行至25min时,曲线发生变化的原因是 。
一、选择题(本题包括18小题,每小题2分,共36分)
1
2
3
4
5
6
7
8
9
B
D
B
B
A
D
B
C
A
10
11
12
13
14
15
16
17
18
D
A
C
B
A
D
D
B
C
二、填空题(本题包括6小题,共64分)
(2)
(3) ①如2Na+2H2O = 2Na++2OH-+H2↑;
②如H++NH3×H2O = NH4++H2O;
③如Al3++3H2O Al(OH)3+3H+;
Al(OH)3+3H+;
20.(10分)(1)铼元素在自然界的存在分散,矿石中含量低,难于富集;铼元素与其他元素共存,难以分离(4分)(2)222(2分)
21.(8分)(1)吸热(2)1/9,1/7(3)2NO+O2+4CO = 4CO2+N2
22.(16分)(每空2分)(1)Al(OH)3+OH-=AlO2-+2H2O (2)
(3)①酸 ② Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
(4)SO2+Cl2+2H2O=H2SO4+2HCl (5)HCl>H2S
(6)S2->Cl->Na+>Al3+ (7)Cl2O7(l)+H2O(l)=2HClO4(aq) △H= -4QkJ/mol
23.(12分)步骤一:(1)①正 (1分);②Cu2++2e = Cu (2分);(2)变小(1分)
步骤二:(一)①3Ag + 4H+ + NO3― = 3Ag+ + NO↑+ 2H2O(2分);
②浓盐酸含有大量氯离子,Au3+ 离子与氯离子形成稳定的AuCl4―离子,使反应2平衡向右移动,则金溶于王水中。(2分)(二)①0.5 (2分);②0.1(2分)
24.(8分)(每空2分)(1) 10Ca(OH)2+10Cl2=2Ca(C1O)2+Ca(C1O3)2+7CaCl2+10H2O
(2) 5 (3)Ⅰ < ; Ⅱ 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com