
ĖâÄŋÁÐąí(°üĀĻīð°ļšÍ―âÎö)
―ņÓÐX(g)ĢŦY(g)![]() 2Z(g)ĢĻÕý·īÓĶΊ·ÅČČ·īÓĶĢĐĢŽīÓ·īÓĶŋŠĘžūđý
2Z(g)ĢĻÕý·īÓĶΊ·ÅČČ·īÓĶĢĐĢŽīÓ·īÓĶŋŠĘžūđý![]() sšóīïĩ―Æ―šâŨīĖŽĢŽ
sšóīïĩ―Æ―šâŨīĖŽĢŽ![]() sĘąÓÉÓÚĖõžþļÄąäĢŽÆ―šâĘÜĩ―ÆÆŧĩĢŽÔÚ
sĘąÓÉÓÚĖõžþļÄąäĢŽÆ―šâĘÜĩ―ÆÆŧĩĢŽÔÚ![]() sĘąÓÖīïĩ―Æ―šâĢŪļųūÝÏÂÍžŧØīðĢšīÓ
sĘąÓÖīïĩ―Æ―šâĢŪļųūÝÏÂÍžŧØīðĢšīÓ![]() sĩ―
sĩ―![]() sžäĩÄĮúÏßąäŧŊĘĮÓÉÄÄÖÖĖõžþŌýÆðĩÄĢĻ ĢĐ
sžäĩÄĮúÏßąäŧŊĘĮÓÉÄÄÖÖĖõžþŌýÆðĩÄĢĻ ĢĐ
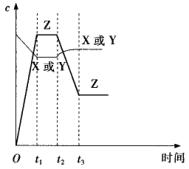
AĢŪÔöīóXŧōYĩÄÅĻķČ
BĢŪÔöīóŅđĮŋ
CĢŪÔöīóZĩÄÅĻķČ
DĢŪÉýļßÎÂķČ
AĢŪÔöīóXŧōYĩÄÅĻķČ
BĢŪÔöīóŅđĮŋ
CĢŪÔöīóZĩÄÅĻķČ
DĢŪÉýļßÎÂķČ
 ―ņÓзīÓĶXĢĻgĢĐĢŦYĢĻgĢĐ
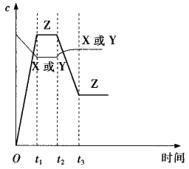
―ņÓзīÓĶXĢĻgĢĐĢŦYĢĻgĢĐ![]() 2ZĢĻgĢĐĢĻÕý·īÓĶ·ÅČČĢĐĢŽÓŌÍžąíĘūļ÷īÓĶÔÚt1Ęąīïĩ―Æ―šâĢŽÔÚt2ĘąŌōļÄąäÄģļöĖõžþķø·ĒÉúąäŧŊĩÄĮúÏߥĢÔōÏÂÍžÖÐĩÄt2ĘąļÄąäĩÄĖõžþĘĮĢĻ ĢĐ
2ZĢĻgĢĐĢĻÕý·īÓĶ·ÅČČĢĐĢŽÓŌÍžąíĘūļ÷īÓĶÔÚt1Ęąīïĩ―Æ―šâĢŽÔÚt2ĘąŌōļÄąäÄģļöĖõžþķø·ĒÉúąäŧŊĩÄĮúÏߥĢÔōÏÂÍžÖÐĩÄt2ĘąļÄąäĩÄĖõžþĘĮĢĻ ĢĐ
AĢŪ ÉýļßÎÂķČŧō―ĩĩÍYĩÄÅĻķČ
BĢŪ žÓČëīßŧŊžÁŧōÔöīóXĩÄÅĻķČ
CĢŪ ―ĩĩÍÎÂķČŧōÔöīóYĩÄÅĻķČ
DĢŪ ËõÐĄĖåŧýŧō―ĩĩÍXĩÄÅĻķČ
(6·Ö)ŋÉÄæ·īÓĶĒŲX(g)ĢŦ2Y(g)  2Z(g) ĄĒĒÚ2M(g)
2Z(g) ĄĒĒÚ2M(g)  N(g)ĢŦP(g)·ÖąðÔÚÃÜąÕČÝÆũĩÄÁ―ļö·īÓĶĘŌÖÐ―øÐÐĢŽ·īÓĶĘŌÖŪžäÓÐÎÞÄĶēÁĄĒŋÉŧŽķŊĩÄÃÜ·âļô°åĄĢ·īÓĶŋŠĘžšÍīïĩ―Æ―šâŨīĖŽĘąÓÐđØÎïĀíÁŋĩÄąäŧŊČįÍžËųĘūĢš
N(g)ĢŦP(g)·ÖąðÔÚÃÜąÕČÝÆũĩÄÁ―ļö·īÓĶĘŌÖÐ―øÐÐĢŽ·īÓĶĘŌÖŪžäÓÐÎÞÄĶēÁĄĒŋÉŧŽķŊĩÄÃÜ·âļô°åĄĢ·īÓĶŋŠĘžšÍīïĩ―Æ―šâŨīĖŽĘąÓÐđØÎïĀíÁŋĩÄąäŧŊČįÍžËųĘūĢš
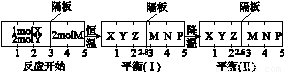
ÔōX(g)ĢŦ2Y(g)  2Z(g)Õý·īÓĶΊ
·īÓĶĢĻĖ·ÅČČĄąŧōĄ°ÎüČČĄąĢĐīïĩ―Æ―šâ(Ēņ)ĘąXĩÄŨŠŧŊÂĘΊ
ĢĻąĢÁôÐĄĘýĩãšóÁ―ÎŧĘýŨÖĢŽÏÂÍŽĢĐĢŧžŲÉčÆ―šâ(Ēņ)ĘąŨóąßČÝÆũĢĻXĄĒYĄĒZĩÄĖåÏĩĢĐĩÄĖåŧýΊ2LĢŽĮóīËÎÂķČÏÂĩÄŧŊŅ§Æ―šâģĢĘý
2Z(g)Õý·īÓĶΊ
·īÓĶĢĻĖ·ÅČČĄąŧōĄ°ÎüČČĄąĢĐīïĩ―Æ―šâ(Ēņ)ĘąXĩÄŨŠŧŊÂĘΊ
ĢĻąĢÁôÐĄĘýĩãšóÁ―ÎŧĘýŨÖĢŽÏÂÍŽĢĐĢŧžŲÉčÆ―šâ(Ēņ)ĘąŨóąßČÝÆũĢĻXĄĒYĄĒZĩÄĖåÏĩĢĐĩÄĖåŧýΊ2LĢŽĮóīËÎÂķČÏÂĩÄŧŊŅ§Æ―šâģĢĘý
(6·Ö)ŋÉÄæ·īÓĶĒŲX(g)ĢŦ2Y(g) 2Z(g) ĄĒĒÚ2M(g)
N(g)ĢŦP(g)·ÖąðÔÚÃÜąÕČÝÆũĩÄÁ―ļö·īÓĶĘŌÖÐ―øÐÐĢŽ·īÓĶĘŌÖŪžäÓÐÎÞÄĶēÁĄĒŋÉŧŽķŊĩÄÃÜ·âļô°åĄĢ·īÓĶŋŠĘžšÍīïĩ―Æ―šâŨīĖŽĘąÓÐđØÎïĀíÁŋĩÄąäŧŊČįÍžËųĘūĢš
ÔōX(g)ĢŦ2Y(g) 2Z(g)Õý·īÓĶΊ ·īÓĶĢĻĖ·ÅČČĄąŧōĄ°ÎüČČĄąĢĐīïĩ―Æ―šâ(Ēņ)ĘąXĩÄŨŠŧŊÂĘΊ ĢĻąĢÁôÐĄĘýĩãšóÁ―ÎŧĘýŨÖĢŽÏÂÍŽĢĐĢŧžŲÉčÆ―šâ(Ēņ)ĘąŨóąßČÝÆũĢĻXĄĒYĄĒZĩÄĖåÏĩĢĐĩÄĖåŧýΊ2LĢŽĮóīËÎÂķČÏÂĩÄŧŊŅ§Æ―šâģĢĘý
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com