
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
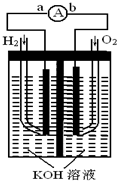 ЃЈ2009?ЬьНђЃЉЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎ
ЃЈ2009?ЬьНђЃЉЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎ
| ||
 ЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎЭМЮЊЕчГиЪОвтЭМЃЌИУЕчГиЕчМЋБэУцЖЦвЛВуЯИаЁЕФВЌЗлЃЌИНЦјЬхЕФФмСІЧПЃЌаджЪЮШЖЈЃЌЧыЛиД№ЃК
ЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎЭМЮЊЕчГиЪОвтЭМЃЌИУЕчГиЕчМЋБэУцЖЦвЛВуЯИаЁЕФВЌЗлЃЌИНЦјЬхЕФФмСІЧПЃЌаджЪЮШЖЈЃЌЧыЛиД№ЃК
| ||
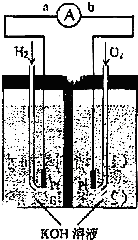
 ЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎШчЭМЮЊЕчГиЪОвтЭМЃЌИУЕчГиЕчМЋБэУцЖЦвЛВуЯИаЁЕФВЌЗлЃЌВЌЮќИНЦјЬхЕФФмСІЧПЃЌаджЪЮШЖЈЃЌЧыЛиД№ЃК
ЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЃЎШчЭМЮЊЕчГиЪОвтЭМЃЌИУЕчГиЕчМЋБэУцЖЦвЛВуЯИаЁЕФВЌЗлЃЌВЌЮќИНЦјЬхЕФФмСІЧПЃЌаджЪЮШЖЈЃЌЧыЛиД№ЃК
| ||
 ЃЈ2010?ЩНЖЋЃЉСђвЛЕтбЛЗЗжНтЫЎжЦЧтжївЊЩцМАЯТСаЗДгІЃК
ЃЈ2010?ЩНЖЋЃЉСђвЛЕтбЛЗЗжНтЫЎжЦЧтжївЊЩцМАЯТСаЗДгІЃК H2+I2
H2+I2 2HIЃЈgЃЉЕФЦНКтГЃЪ§K=
2HIЃЈgЃЉЕФЦНКтГЃЪ§K=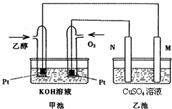
ЬтКХ
1
2
3
4
5
6
7
8
9
Д№АИ
A
D
B
D
C
B
C
B
D
ЬтКХ
10
11
12
13
14
15
16
17
18
Д№АИ
B
D
B
A
A
C
D
B
A
19ЃЎЃЈ1ЃЉCH3CH2OH+4H2SO4  4SO2Ёќ+CO2Ёќ+7H2O+CЃЛ
2Зж
4SO2Ёќ+CO2Ёќ+7H2O+CЃЛ
2Зж
ЃЈ2ЃЉЂмЁњЂлЁњЂйЁњЂкЃЛ 1Зж
ЃЈ3ЃЉЦЗКьЭЪЩЋЃЛ ЛьКЯЦјжагаSO2ЁЃ фхЫЎбеЩЋБфЧГЃЛ
НЋSO2ЮќЪеЭъШЋЁЃ ЛьКЯЦјжавбЮоSO2ЁЃ УППе1Зж
ЃЈ4ЃЉЮоЫЎCuSO4 ЃЌ БЅКЭЪЏЛвЫЎЃЌ УППе1Зж
20ЃЎЃЈ1ЃЉЙ§ТЫ
ЃЈ2ЃЉAl2O3ЃЛ K2SO4КЭЃЈNH4ЃЉ2SO4 УППе1Зж
ЃЈ3ЃЉЂкAl3+ЃЋ3NH3?H2OЃНAl(OH) 3Ё§ЃЋ3NH4+
ЂлNaAlO2ЃЋHClЃЋH2OЃНAl(OH) 3Ё§ЃЋNaCl УППе2Зж
21.
A. CH3 CH3
| |
CH3ЃCЃCH2ЃCЃCH3
| |
CH3 CH3
B1. CH3 CH3
| |
CH3ЃCЃCЃCH2ЃCH3
| |
CH3 CH3
B2. ЁЁЁЁ CH2CH3
|
CH3CH2ЃCЃCH2CH3
|
CH2CH3
B3. CH3 CH3 CH3
| | |
CH3ЃCHЃC ЃCHЃCH3
| УППе2Зж
CH3
22ЃЎЂкЂлЂмЂнЂо ЂмЂо УППе2Зж
23.ЃЈ1ЃЉBnAm 1Зж ЃЈ2ЃЉAn- 1Зж An-+H2O=HAЃЈn-1ЃЉ-+OH- 2Зж
24.ЃЈ1ЃЉH2 ЃЌ O2 ЃЌ O2 + H2O + 4e- = 4OH- H2 ? 2e- + 2OH- = 2H2OЃЛ УППе1Зж
ЃЈ2ЃЉO2 + 2H2O + 4e- = 4OH- ЃЌ CH4 + 10OH- + 8e- = CO32- + 7H2O УППе1Зж
CH4 + 2KOH+ 2O2 = K2CO3 + 3H2OЁЃ 2Зж
25.ЂёЃЈ1ЃЉ CH3COOH +OH-=CH3COO-+H2OЁЃ
ЃЈ2ЃЉ 0.1 ЃЈ3ЃЉ Дѓгк ЃЌ аЁгкЃЌаЁгк
ЃЈ4ЃЉ c (CH3COO- ) >c (Na+) > c (H+)> c (OH ? ) УППе1Зж
 ЂђЃЈ1ЃЉCO32-+H2OHCO3-+OHЃ
ЂђЃЈ1ЃЉCO32-+H2OHCO3-+OHЃ
ЯђДПМюШмвКжаЕЮМгЪ§ЕЮЗгЬЊЪдвККѓЃЌШмвКЯдКьЩЋЃЛШЛКѓж№ЕЮМгШыТШЛЏИЦШмвКжБжСЙ§СПЃЌШєШмвККьЩЋж№НЅБфЧГжБжСЯћЪЇЃЌдђЫЕУїЩЯЪіЙлЕуЁЃ
ЃЈ2ЃЉгУpHЪджНЃЈЛђpHМЦЃЉВтГЃЮТЯТ0.1mol?LЃ1ДПМюШмвКЕФpHЃЌШєpHЃМ12ЃЌдђИУЭЌбЇ
ЕФЙлЕуе§ШЗЃЛШєpHЃО12ЃЌдђИУЭЌбЇЕФЙлЕуВЛе§ШЗЁЃ
ЃЈ3ЃЉBЁЂD УППе1Зж
26ЃЎЃЈ1ЃЉ12.4g 3Зж ЃЈ2ЃЉ49.18ЃЅ 2Зж
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com