
题目列表(包括答案和解析)
某课外活动小组对一氧化碳还原氧化铁的实验中最后的产物产生浓厚的兴趣,试通过实验来探究其成分。
Ⅰ.实验装置:
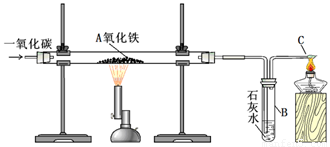
用一氧化碳还原氧化铁的实验装置
该装置B中发生的离子方程式是
装置B的作用是
Ⅱ.实验现象:玻璃管A中的粉末由红色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊。
Ⅲ.实验结论:
甲认为:依据上述实验现象可以判断出生成的黑色固体为金属铁。
乙认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色固体被磁铁吸引。于是得出生成的黑色固体为金属铁的结论。
请你通过该反应的相关资料对他们结论作出判断并通过实验检验其合理性:
(1)在一定条件下:一氧化碳与氧化铁在加热条件下,可发生如下反应
3Fe2O3+CO 2Fe3O4+CO2
2Fe3O4+CO2
Fe3O4+4CO 4Fe+4CO2
4Fe+4CO2
(2)四氧化三铁(Fe3O4)为黑色固体,有强磁性,能够被磁铁吸引。
甲、乙同学的结论: 你对此评价的理由是:
Ⅳ.实验探究
对反应后固体成分提出假设:
假设1:反应后固体中只有Fe;
假设2:反应后固体中只有Fe3O4;
假设3:反应后固体中__ _____________________
为确定实验中最后的产物的成分,丙同学设计如下实验,请您利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置。
限选试剂和仪器: 1mol/LCuSO4 、0.01mol/L KSCN溶液、1mol/L盐酸、0.01mol/L氯水、试管、玻璃棒、胶头滴管。
|
实验操作 |
预期现象和结论 |
|
步骤一:取硬质玻璃管中固体产物少量分别于A、B试管中,加入足量1mol/LCuSO4溶液、搅拌溶解。 |
(1)若A试管中黑色固体不溶解,并且没有观察到其他现象,则黑色固体为 (2)若B试管中有红色固体析出,则说明黑色固体中含有Fe。 |
|
步骤二:对试管B中溶液过滤,将所得固体洗涤干净后,加足量1mol/L盐酸后,再依次分别加入适量0.01mol/L氯水、少量0.01mol/L KSCN溶液 |
(1)若溶液不变红色,则
(2)若溶液变红色,则
|
Ⅴ.延伸探究:丁同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应) (填“行”或“不行”)理由是 。
(1)能跟NaOH溶液反应生成红褐色沉淀,此沉淀不溶于过量的NaOH溶液,_______________________________________。
(2)能跟NaOH溶液反
(3)能跟盐酸反
(4)能跟硫酸溶液反应生成白色沉淀,此沉淀不溶于过量的HNO3,______________________________________。
(5)用稀硫酸酸化后,通入H2S气体,生成黑色沉淀,______________________________。
| 实验操作 | 预期现象 | 结 论 |
| 步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水溶解,分别取少量于A、B试管中 | 固体完全溶解,得到无色透明溶液 | / |
| 步骤二:取试管A,向溶液中加入 |
假设1 或假设3成立;若没有该现象则假设2成立. | |
| 步骤三:取试管B,向其中先加入 再加入 |
产生 再加入试剂看到产生白色沉淀. |
假设3成立.若无白色沉淀产生则假设1成立. |


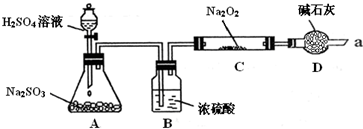
虽然氟元素早在1810年就被发现,但170多年来化学家试图用化学方法制取氟单质的尝试一直未获成功。直到1986年,化学家Karl Christe首次用化学方法制得了F2。他提出的三步反应如下(反应①、②里氟元素化合价不变):
① KMnO4 + KF + H 2O2 + HF → K2Mn F6 + ____________ + H2O
2O2 + HF → K2Mn F6 + ____________ + H2O
② SbCl5 + HF → SbF5 + ____________
③ 2K2MnF6 + 4SbF5 → 4KSbF6 + 2MnF3 + F2↑
请根据以上反应回答问题:
(1)反应①中空格上应填物质的化学式为______________,为什么填这一物质,试用氧化还原反应理论解释_______________________________________。
(2)完成反应②:_______________________________________________ 。
。 (3)反应③中的氧化剂为________________,被氧化的元素为________________。
(3)反应③中的氧化剂为________________,被氧化的元素为________________。
(4)配平反应①,并标出电子转移的方向和数目。(将答案写在下面空格上)
________________________________________________________。
说明:
1. 本答案供阅卷评分使用,试题的参考解答是用来说明评分标准的,考生如按其他方法或步骤解答,正确的同样给分;有错的,根据错误的性质,参照评分标准中相应的规定评分。
2. 化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3. 化学方程式、离子方程式未配平的,都不给分。
4. 计算只有最后答案而无演算过程的,不给分。
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. A 2. D 3. B 4. A 5. C 6. D 7. C 8. C 9. D 10. D 11. B 12. C 13. B 14. D 15. A 16. D 17. A 18. C 19. A 20. B 21. B 22. D 23. B 24. C 25. A
第Ⅱ卷(非选择题,共50分)
二、(本题包括4小题,共22分)
26.(共4分)3,28,9,1,14(2分) 0.1(2分)
27.(共6分,每空2分)(1)0.01 mol/(L?s) (2)> 乙
 28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
O2+2H2O+4e-===4OH-
29.(共9分,每空1分)(1)AlCl3 Al2O3 Fe
(2)铝热 焊接钢轨,冶炼钒、铬、锰等金属(答出一种即可)
(3)3Fe+4H2O高温====Fe3O4+4H2
(4)① 2Al+2OH-+2H2O===2AlO-2+3H2↑ ② Al3++3AlO-2+6H2O===4Al(OH)3↓
(5)氨水
三、(本题包括2小题,共15分)
30.(共7分)(1)I-、Fe2+、Al3+(3分) HCO-3、NO-3(2分)
(2)4Fe(OH)2+O2+2H2O===4Fe(OH)3(1分)
(3)AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3(1分)
31.(共8分,每空1分)(1)Mg2++2OH-===Mg(OH)2↓(1分)
(2)碱式滴定管、酸式滴定管(1分) (3)酚酞(1分) 酚酞的变色范围最接近中性,滴定终点时,pH为8.2~10,Mg(OH)2不会溶解,不影响测定结果(1分)
(4)偏低(2分) (5)7.5 %(2分)
四、(本题包括2小题,共13分)
32.(共4分)解:n(Cu)==0.09 mol,n(HNO3)=2.0 mol/L×
==
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O ………………………………(1分)
3 8
=
因为< 所以硝酸过量 ……………………………………(1分)
n(NO)=×n(Cu)=×0.09 mol=0.06 mol ……………………………………(1分)
溶液中n(NO-3)=0.3 mol-0.06 mol=0.24 mol
c(NO-3)==1.6 mol/L ……………………………………………………(1分)
答:溶液中NO-3 的物质的量浓度为1.6 mol/L。
(此题的评分原则是:判断过量2分,算出NO-3 的浓度2分)
 33.(共9分)解:合金溶解于盐酸时所发生的反应有:
33.(共9分)解:合金溶解于盐酸时所发生的反应有:
Mg+2HCl===MgCl2+H2↑,2Al+6HCl===2AlCl3+3H2↑ ………………(1分)
根据图示,加NaOH溶液至130 mL过程中,发生的反应为:
NaOH+HCl===NaCl+H2O MgCl2+2NaOH===Mg(OH)2↓+2NaCl
AlCl3+3NaOH===Al(OH)3↓+3NaCl ………………………………………(1分)
当NaOH溶液由130 mL加至150 mL时,发生的反应为:
Al(OH)3+NaOH===NaAlO2+2H2O …………………………………………(1分)
(1)n(Mg)=n[Mg(OH)2]==0.15 mol ………………………………(1分)
m(Mg)=0.15 mol×
n(Al)=n[Al(OH)3]==0.1 mol ……………………………………(1分)
m(Al)=0.1 mol×
(2)据题意,在加入NaOH溶液130 mL时,溶液中n(Na+)=n(Cl-) …………(1分)
Na+ 全部来自NaOH,Cl- 全部来自盐酸,故n(HCl)=130×10
c(HCl)==6.5 mol/L …………………………………………………(1分)
答:原合金中Al、Mg的质量分别是
(此题的评分原则是:化学方程式或离子方程式共3分,算出铝的质量2分,算出镁的质量2分,算出盐酸的浓度2分。如未写化学方程式或离子方程式,计算结果正确者,镁、铝的质量各3分,盐酸的浓度3分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com