
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
2KNO3![]() 2KNO2ΘΪO2Γϋ
2KNO2ΘΪO2Γϋ
2Cu(NO3)2![]() 2CuOΘΪ4NO2ΓϋΘΪO2Γϋ
2CuOΘΪ4NO2ΓϋΘΪO2Γϋ
2AgNO3![]() 2AgΘΪ2NO2ΓϋΘΪO2Γϋ
2AgΘΪ2NO2ΓϋΘΪO2Γϋ
œ÷ΫΪΗΟΙΧΧεΈο÷ Φ”»»Ζ÷ΫβΘ§ΒΟΒΫn LΤχΧεΘ§ΫΪ’β–©ΤχΧεΆ®ΙΐΉψΝΩΒΡΥ°ΚσΜΙ Θ”ύ![]() LΤχΧε(ΤχΧεΧεΜΐ‘ΎœύΆ§Ή¥Χ§œ¬≤βΕ®Θ§«“≤ΜΩΦ¬«NO2ΨέΚœ≥…N2O4ΒΡ«ιΩω)ΓΘ
LΤχΧε(ΤχΧεΧεΜΐ‘ΎœύΆ§Ή¥Χ§œ¬≤βΕ®Θ§«“≤ΜΩΦ¬«NO2ΨέΚœ≥…N2O4ΒΡ«ιΩω)ΓΘ
(1)»τΗΟΙΧΧε÷–÷ΜΚ§“Μ÷÷Έο÷ Θ§‘ρΗΟΈο÷ «___________(ΧνΜ·―ß ΫΘ§œ¬Ά§)ΘΜ
(2)»τΗΟΙΧΧε÷–Κ§ΝΫ÷÷Έο÷ Θ§‘ρΗΟΝΫ÷÷Έο÷ «_______ΓΔ_______Θ§ΤδΈο÷ ΒΡΝΩ÷°±»ΈΣ_______ΘΜ
(3)»τΗΟΙΧΧε÷–Κ§»Ϊ≤Ω»ΐ÷÷Έο÷ Θ§‘ρ»ΐ÷÷Έο÷ ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ_________ΓΘ
ΙΧΧεœθΥα―ΈΦ”»»“ΉΖ÷Ϋβ«“≤ζΈοΫœΗ¥‘”ΓΘ“―÷ΣKNO3ΓΔCu(NO3)2ΓΔAgNO3»ΐ÷÷œθΥα―ΈΒΡ»»Ζ÷ΫβΖ¥”ΠΖΫ≥Χ Ϋ»γœ¬ΘΚ
IΘ°2KNO3 2KNO2ΘΪO2Γϋ
2KNO2ΘΪO2Γϋ
IIΘ°2Cu(NO3)
2  2CuOΘΪ4NO2ΓϋΘΪO2Γϋ
2CuOΘΪ4NO2ΓϋΘΪO2Γϋ
IIIΘ°2AgNO3 2AgΘΪ2NO2ΓϋΘΪO2Γϋ
2AgΘΪ2NO2ΓϋΘΪO2Γϋ
(1)Ρ≥ΙΧΧεΩ…Ρή”…KNO3ΓΔCu(NO3)2ΓΔAgNO3»ΐ÷÷œθΥα―Έ÷–ΒΡ“Μ÷÷ΜρΦΗ÷÷Ήι≥…ΓΘ»Γ ΝΩΗΟΙΧΧε≥δΖ÷Φ”»»Θ§ΒΟΒΫ“ΜΕ®ΝΩΤχΧεΓΘ»τΗΟΤχΧεΨ≠Υ°≥δΖ÷Έϋ ’ΚσΘ§ Θ”ύΤχΧεΒΡΧεΜΐ‘ΎΆ§Έ¬Ά§―Ιœ¬ΈΣΈϋ ’«ΑΒΡ1/6ΓΘ (Κω¬‘―θ‘ΎΥ°÷–ΒΡ»ήΫβ)
ΔΌ»τΗΟΙΧΧε÷Μ «”…“Μ÷÷―ΈΉι≥…Θ§‘ρΗΟ―ΈΈΣ ΓΘ
ΔΎ»τΗΟΙΧΧε «ΜλΚœΈοΘ§‘ρΗΟΜλΚœΈοΒΡΩ…ΡήΉι≥…ΈΣ ΓΘ
(2)Ρ≥―ßœΑ–ΓΉι“‘Mg(NO3)2ΈΣ―–ΨΩΕ‘œσΘ§Ά®Ιΐ Β―ιΧΫΨΩΤδ»»Ζ÷ΫβΒΡ≤ζΈοΘ§…ηΦΤ»γœ¬ΆΦΥυ ΨΒΡ Β―ιΉΑ÷ΟΘ®ΆΦ÷–Φ”»»ΓΔΦ–≥÷“«ΤςΒ»Ψυ Γ¬‘Θ©ΘΚ

ΓΨ Β―ι≤Ϋ÷ηΓΩ
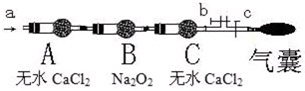
aΘ°“«ΤςΝ§Ϋ”ΚσΘ§Ζ≈»κΙΧΧε ‘ΦΝ÷°«ΑΘ§ΙΊ±’kΘ§ΈΔ»»”≤÷ ≤ΘΝßΙήAΓΘ
bΘ°≥Τ»ΓMg(NO3)2ΙΧΧε3.7g÷Ο”ΎA÷–Θ§œ»Ά®»κ“ΜΕΈ ±ΦδN2Θ§‘ΌΙΊ±’kΘ§”ΟΨΤΨΪΒΤΦ”»»”≤÷ ≤ΘΝßΙήAΓΘ
cΘ°¥ΐ―υΤΖΆξ»ΪΖ÷ΫβΘ§A ΉΑ÷Οά以÷Ν “Έ¬ΓΔ≥ΤΝΩΘ§≤βΒΟ Θ”ύΙΧΧεΒΡ÷ ΝΩΈΣ1.0g ΓΘ
ΔΌ≤Ϋ÷ηaΒΡΡΩΒΡ « ΘΜ
ΔΎ“άΨί“―÷ΣΒΡ»ΐΗωΖΫ≥Χ ΫΘ§‘ΌΗυΨί Θ”ύΙΧΧεΒΡ÷ ΝΩ–¥≥ωMg(NO3)2»»Ζ÷ΫβΖΫ≥Χ ΫΈΣΘΚ ΓΘ
Δέ»τA÷–ΙΧΧεΈΣAgNO3Θ§”Ο“‘…œ Β―ιΉΑ÷ΟΫχ–– Β―ι ±Θ§D ÷–ΒΡœ÷œσΈΣ Θ§”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ≥ωœ÷ΗΟœ÷œσΒΡ‘≠“ρΘΚ_____________________ ΓΘ
Δή¥” Β―ιΑ≤»ΪΒΡΫ«Ε»≈–ΕœΗΟ Β―ιΉΑ÷Ο”–Έό»±œίΘΩ»τ”–Θ§”Π»γΚΈΗΡΫχΘΩ ΓΘ
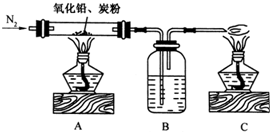 Θ®2009?ΙψΕΪΡΘΡβΘ©Ρ≥ΩΈΆβ–ΓΉι”ϊΆ®Ιΐ Β―ι÷ΛΟςΖΫ«ΠΩσΖ÷ΫβΥυΒΟΑΉ…ΪΖέΡ©÷–Κ§”–―θ‘ΣΥΊΘ§…ηΦΤ“‘œ¬ΒΡ Β―ιΉΑ÷ΟΘΚ
Θ®2009?ΙψΕΪΡΘΡβΘ©Ρ≥ΩΈΆβ–ΓΉι”ϊΆ®Ιΐ Β―ι÷ΛΟςΖΫ«ΠΩσΖ÷ΫβΥυΒΟΑΉ…ΪΖέΡ©÷–Κ§”–―θ‘ΣΥΊΘ§…ηΦΤ“‘œ¬ΒΡ Β―ιΉΑ÷ΟΘΚ
| ||
| ||
| ||
| ||
| AΓΔ4CuOΘ®sΘ©®T2Cu2OΘ®sΘ©+O2Θ®gΘ©‘Ύ “Έ¬œ¬≤ΜΡήΉ‘ΖΔΫχ––Θ§ΥΒΟςΗΟΖ¥”ΠΓςHΘΦ0 | BΓΔ…ζΧζΚΆ¥ΩΧζΆ§ ±Ζ≈»κΚΘΥ°÷–Θ§¥ΩΧζΗϋ“ΉΗ· ¥ | CΓΔ≥ΘΈ¬œ¬Θ§PbSO4“Ή»ή”ΎpH=7ΒΡCH3COONH4»ή“ΚΘ§ΥΒΟςΘ®CH3COOΘ©2Pb «»θΒγΫβ÷ | DΓΔH2SΘ®gΘ©+FeOΘ®sΘ©?FeSΘ®sΘ©+H2OΘ®gΘ©Θ§ΤδΥϊΧθΦΰ≤Μ±δ ±‘ω¥σ―Ι«ΩΘ§Ζ¥”ΠΥΌvΘ®H2SΘ©ΚΆH2SΒΡΤΫΚβΉΣΜ·¬ Ψυ‘ω¥σ |
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com