课外化学兴趣小组欲测定铜锌合金粉末中锌的质量分数.
Ⅰ.除托盘天平必用外,供选择的实验装置如下:
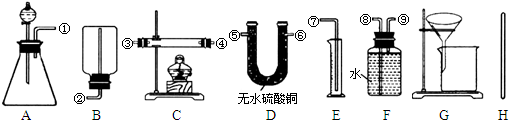
Ⅱ.实验中可测得的数据及其代号如下:
样品的质量m
1;充分反应生成的气体体积V(标准状况);反应前仪器和药品的总质量m
2;充分反应后仪器和药品的总质量m
3;充分反应后剩余固体的质量m
4.
(1)实验时必须用到的化学试剂为
稀硫酸
稀硫酸
.
(2)甲同学实验中使用了A、E、F三种装置,组装时接口编号的连接顺序为:
①⑨⑧⑦
①⑨⑧⑦
.样品中锌的质量分数的计算式为
.
(3)乙同学实验中测得的数据为m
1和m
4,他使用的实验装置有
AGH
AGH
(填字母).
(4)丙同学实验中只选用了A装置,他要测得的数据有
m1、m2、m3
m1、m2、m3
(填代号).
(5)丁同学设计了另一种测定方法,他考虑使用A、C、D三种装置,在C装置中添加足量CuO.除测定m
1外,还准备测定C装置反应前后的质量变化.请评价该方法是否可行并说明理由:
不可行;因为氢气还原氧化铜时,排除装置中的空气及冷却装置都要消耗氢气,而且部分氢气未反应即排出,所以不可能通过计算得出氢气的产量,也无法计算锌的质量
不可行;因为氢气还原氧化铜时,排除装置中的空气及冷却装置都要消耗氢气,而且部分氢气未反应即排出,所以不可能通过计算得出氢气的产量,也无法计算锌的质量
.

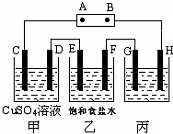 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、G、H 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、G、H 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
