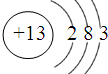
有A、B、C、D、E五种短周期主族元素,A、B、C、D原子序数依次增大,原子半径按D、A、B、C、E依次减小,A、B的核电荷数之和等于D的核电荷数,D的最外层电子数为C的最外层电子数的一半,E可以分别与A、B、C形成电子总数相同的共价分子.
(1)写出元素D在周期表中的位置
第三周期ⅢA族
第三周期ⅢA族
.
(2)元素A的非金属
<
<
(填“>”或“<”)元素C.
(3)C离子与D离子的电子数相等,比较这两种离子的半径大小:C离子
>
>
(填“>”或“<”)D离子.
(4)写出由元素A和元素E组成的10电子分子的电子式
.
(5)氧化铜与D的单质在高温下发生化学反应的方程式
,若得到1mol氧化产物,则该反应转移电子
6
6
mol.取该反应的还原产物3.2g与12.5mL、8mol/L的硫酸溶液(98%的硫酸其物质的量的浓度为18mol/L)混合,按如图装置进行实验,实验发现,3.2g还原产物几乎被消耗掉,请你解释其原因
由于酒精灯一直在加热,随着反应进行,反应生成的水不断蒸发,Cu和硫酸的反应在持续进行,而Cu和H2SO4的物质的量之比又恰好是1:2
由于酒精灯一直在加热,随着反应进行,反应生成的水不断蒸发,Cu和硫酸的反应在持续进行,而Cu和H2SO4的物质的量之比又恰好是1:2
.






 在一定条件下可实现下图所示物质之间的变化:
在一定条件下可实现下图所示物质之间的变化: 有A、B、C、D、E五种短周期主族元素,A、B、C、D原子序数依次增大,原子半径按D、A、B、C、E依次减小,A、B的核电荷数之和等于D的核电荷数,D的最外层电子数为C的最外层电子数的一半,E可以分别与A、B、C形成电子总数相同的共价分子.
有A、B、C、D、E五种短周期主族元素,A、B、C、D原子序数依次增大,原子半径按D、A、B、C、E依次减小,A、B的核电荷数之和等于D的核电荷数,D的最外层电子数为C的最外层电子数的一半,E可以分别与A、B、C形成电子总数相同的共价分子.

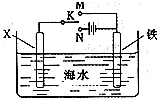 铁、铝是现代金属材料的主角.
铁、铝是现代金属材料的主角.