π˝ÃºÀ·ƒ∆£®Na
2CO
4£©‘⁄œ¥µ”°¢”°»æ°¢‘Ï÷Ω°¢“Ω“©Œ¿…˙µ»¡Ï”Ú”–¥Û¡ø”¶”√£Æ
“—÷™£∫π˝ÃºÀ·ƒ∆”ΡÚÀ·»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã Ω»Áœ¬£∫
Na
2CO
4+H
2SO
4°˙Na
2SO
4+H
2O
2+CO
2°¸ 2H
2O
2°˙2H
2O+O
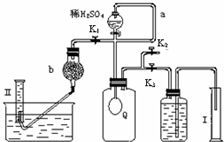
2°¸Œ™≤‚∂®“—±‰÷ µƒπ˝ÃºÀ·ƒ∆£®∫¨ÃºÀ·ƒ∆£©µƒ¥ø∂»£¨…˺∆»ÁÕºÀ˘ 浃 µ—È£∫QŒ™-æþ”–¡º∫√µƒµØ–‘µƒ∆¯«Ú£®≤ª”Î∑¥”¶ŒÔ∫Õ…˙≥…ŒÔ∑¥”¶£©£¨≥∆»°“ª∂®¡øµƒ—˘∆∑∫Õ…Ÿ¡ø∂˛—ıªØ√Ã∑≈”⁄∆‰÷–£¨∞¥Õº∞≤◊∞∫√ µ—È◊∞÷√£¨¥Úø™∑÷“∫¬©∂∑µƒªÓ»˚£¨Ω´œ°H
2SO
4µŒ»Î∆¯«Ú÷–£Æ
£®1£©Qƒ⁄∑¢…˙∑¥”¶…˙≥…µƒ∆¯ÃÂŒ™
CO2°¢O2
CO2°¢O2
£ÆµºπÐa◊˜”√ «
∆Ω∫‚∑÷“∫¬©∂∑…œ°¢œ¬µƒ—π«ø£¨ πœ°H2SO4À≥¿˚µŒœ¬
∆Ω∫‚∑÷“∫¬©∂∑…œ°¢œ¬µƒ—π«ø£¨ πœ°H2SO4À≥¿˚µŒœ¬
£Æ
£®2£©Œ™≤‚≥ˆ∑¥”¶ ±…˙≥…∆¯Ãµƒ◊Ðê˝£¨µŒœ°H
2SO
4«∞±ÿ–Îπÿ±’K
1°¢K
2£¨¥Úø™K
3£Æµ±…œ ˆ∑¥”¶Õ£÷π£¨Ω´K
1°¢K
2°¢K
3¥¶”⁄πÿ±’◊¥Ã¨£¨»ª∫Ûœ»¥Úø™K
2£¨‘Ÿª∫ª∫¥Úø™K
1£¨’‚ ±ø…π€≤ÏµΩµƒœ÷œÛ «
∆¯«ÚQ¬˝¬˝Àı–°£¨◊Û≤ýµºπД–∆¯≈ð…˙≥…
∆¯«ÚQ¬˝¬˝Àı–°£¨◊Û≤ýµºπД–∆¯≈ð…˙≥…
£¨b÷–◊∞µƒºÓ ت“µƒ◊˜”√ «
Œ¸ ’∂˛—ıªØú
Œ¸ ’∂˛—ıªØú
£Æ
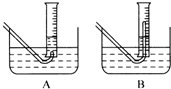
£®3£© µ—ÈΩ· ¯ ±£¨¡øÕ≤I÷–”–xmLÀÆ£¨¡øÕ≤¢Ú÷– ’ºØµΩymL∆¯Ã£®…œ ˆÃª˝æ˘“—’€À„µΩ±Í◊º◊¥øˆ£©£¨‘Úπ˝ÃºÀ·ƒ∆µƒ¥ø∂» «
£® Ω¡ø£∫Na
2CO
4-122£¨Na
2CO
3-106£©£Æ
£®4£©ƒ≥Õ¨—ß µ—È≤‚µ√µƒπ˝ÃºÀ·ƒ∆µƒ¥ø∂»≥¨π˝100%£¨ƒ„»œŒ™ø…ƒÐµƒ‘≠“Ú «
BC
BC
A£Æ∆¯ÃÂ÷Õ¡Ù‘⁄Q∫Õµº∆¯πÐ÷–£¨Œ¥»´≤øΩ¯»Î¡øÕ≤¢Ú
B£Æ¡øÕ≤¢Ú∂¡ ˝ ±£¨¡øÕ≤“∫√Ê∏þ”⁄ÀÆ≤€“∫√Ê
C£Æ”“≤ý¡øÕ≤¢Ò∫Õ¥¢“∫ºØ∆¯∆ø¡¨Ω”µºπЃ⁄µƒ“∫ÃÂ√ª”–º∆»Î∂¡ ˝x
D£Æ∆¯ÃÂê˝ ˝÷µx°¢y√ª”–ø€≥˝µŒº”µƒ¡ÚÀ·µƒÃª˝£Æ


 π˝ÃºÀ·ƒ∆£®Na2CO4£©‘⁄œ¥µ”°¢”°»æ°¢‘Ï÷Ω°¢“Ω“©Œ¿…˙µ»¡Ï”Ú”–¥Û¡ø”¶”√£Æ
π˝ÃºÀ·ƒ∆£®Na2CO4£©‘⁄œ¥µ”°¢”°»æ°¢‘Ï÷Ω°¢“Ω“©Œ¿…˙µ»¡Ï”Ú”–¥Û¡ø”¶”√£Æ