
题目列表(包括答案和解析)
已知25℃时有关弱酸的电离平衡常数:
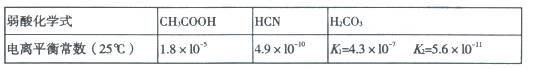
下列有关说法正确的是( )
A.NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-)
B.1 mol·L-1HCN溶液与1mol·L-1 NaOH溶液等体积混合后,测得所得溶液显酸性
C.等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
D.1mol/L醋酸溶液加水稀释,所有离子浓度均减小
A.pH=2与pH=1的硝酸中c(H+)之比为1:10
B.Na2CO3溶液中c(Na+)与c(![]() )之比为2:1
)之比为2:1
C.0.2mol/L与0.1mol/L醋酸中c(H+)之比为2:1
D.NO2溶于水,被氧化的n(NO2)与被还原的n(NO2)之比为3:1
已知25℃时有关弱酸的电离平衡常数:
下列有关说法正确的是( )
| A.NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) |
| B.1 mol·L-1HCN溶液与1mol·L-1 NaOH溶液等体积混合后,测得所得溶液显酸性 |
| C.等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| D.1mol/L醋酸溶液加水稀释,所有离子浓度均减小 |
常温下,0.1mol/L醋酸溶液的pH=3。将该温度下0.2 mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后,混合液的pH=4.7,下列说法正确的是:
A.该温度下,0.0lmol/L醋酸溶液的pH=4
B.该温度下,用0.1mol/L醋酸和0.01 mol/L醋酸分别完全中和等体积0.1 mol/L的NaOH溶液,消耗两醋酸的体积比为1∶10
C.该温度下,0.01mol/L醋酸溶液中由水电离出的c(H+)=10-11mol/L
D.该温度下,0.2mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后,混合液中c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com