
题目列表(包括答案和解析)
工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
 △H=-15.73kJ·mol-1
△H=-15.73kJ·mol-1
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) △H= +640.4kJ·mol-1
则反应Fe2O3(s)+CO(g) = 2FeO(s)+CO2(g) 的△H= 。
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解)。写出电解总方程式 。
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的 极发生 反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为 ,消耗硫酸的物质的量是 。
(共10分)
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。
①图中所示反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”、“不需要”或“不一定”)加热,该反应的△H = (用含E1、E2的代数式表示)。
②对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因是____________________________________。
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ ①C(s)+O2(g) === CO2(g) ΔH1<0
途径Ⅱ 先制水煤气:②C(s)+H2O(g) === CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
③2CO(g)+O2(g) === 2CO2(g) ΔH3<0 ④2H2(g)+O2(g) === 2H2O(g) ΔH4<0
请回答下列问题:
①判断两种途径放热:途径Ⅰ放出的热量________途径Ⅱ放出的热量(填“大于”、“等于”或“小于”)。
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系是_________________________________。
③由于制取水煤气的反应里,反应物具有的总能量________(填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________能量才能转化为生成物,因此其反应条件为________。
(3)已知:Fe2O3(s)+3CO(g) === 2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g) === 2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g) === 3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
请写出CO还原FeO的热化学方程式:______________________________________。
钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如下图:

(1)铁在元素周期表中位于 周期 族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有: (选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是 。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
|
反应序号 |
化学反应 |
反应热 |
|
① |
Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g) |
△H1= -26.7kJ·mol-1 |
|
② |
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) |
△H2= -50.8kJ·mol-1 |
|
③ |
Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g) |
△H3= -36.5kJ·mol-1 |
|
④ |
FeO(s)+CO(g)=Fe(s)+CO2(g) |
△H4 |
反应④△H4= kJ·mol-1。
(5)1100℃时, FeO(s)+CO(g)  Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为:
。
Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为:
。
(14分)钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如下图:
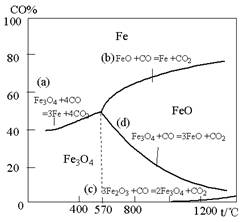
(1)铁在元素周期表中位于 周期 族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有: (选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是 。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
|
反应序号 |
化学反应 |
反应热 |
|
① |
Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g) |
△H1= -26.7kJ·mol-1 |
|
② |
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) |
△H2= -50.8kJ·mol-1[来源:学.科.网] |
|
③ |
Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g)[来源:学+科+网] |
△H3= -36.5kJ·mol-1 |
|
④ |
FeO(s)+CO(g)=Fe(s)+CO2(g) |
△H4 |
反应④△H4= kJ·mol-1。
已知下列热化学方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
Fe2O3(s)+ CO(g)===
CO(g)===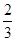 Fe3O4(s)+
Fe3O4(s)+ CO2(g) ΔH=-15.73 kJ/mol
CO2(g) ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
则14 g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的ΔH约为( )
A.-218 kJ/mol B.-109 kJ/mol C.+218 kJ/mol D.+109 kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com