
题目列表(包括答案和解析)
(1)在实验室中作小型实验:把物质A、B按一定比例充入一个表面积为![]() 的圆柱形容器,使压强为P,然后将整个体系用加热器加热到280℃,发生如下反应
的圆柱形容器,使压强为P,然后将整个体系用加热器加热到280℃,发生如下反应![]() ,若平均每分钟生成0.5 mol的C,容器表面向外散热速率平均为
,若平均每分钟生成0.5 mol的C,容器表面向外散热速率平均为![]() 为了维持恒温280℃,平均每分钟需用加热器向容器提供多少kJ的热量.(简述推理过程)
为了维持恒温280℃,平均每分钟需用加热器向容器提供多少kJ的热量.(简述推理过程)
答:_________________________________________.
(2)若将(1)的小型实验扩大为工业生产:将反应容器的底面半径和高度都扩大到原容器的10倍,做成“相似体”,并向其中将A、B按原比例充入,使压强仍为P,然后加热到280℃使反应开始.为了维持恒温280℃,反应开始后,应继续加热还是进行冷却?(设容器表面散热速率不变)
平均每分钟用加热器向体系提供或者用冷却器吸收了多少kJ的热量.(简述推理过程)
答:________________________________________.
(3)在恒温、恒压下,向(2)的“相似体”平衡体系中将A、B按原比例充入,重新达到平衡时,C的体积分数_________.
 的圆柱形容器,使压强为P,然后将整个体系用加热器加热到280℃,发生如下反应
的圆柱形容器,使压强为P,然后将整个体系用加热器加热到280℃,发生如下反应 ,若平均每分钟生成0.5 mol的C,容器表面向外散热速率平均为
,若平均每分钟生成0.5 mol的C,容器表面向外散热速率平均为 ,为了维持恒温280℃,平均每分钟需用加热器向容器提供多少kJ的热量.(简述推理过程)
,为了维持恒温280℃,平均每分钟需用加热器向容器提供多少kJ的热量.(简述推理过程) (1)在实验室中做小型实验:把物质A、B按一定比例充入一个表面积为300 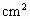 的圆形容器中,使压强为p,然后将整个体积用加热器加热到280℃时,发生如下反应:
的圆形容器中,使压强为p,然后将整个体积用加热器加热到280℃时,发生如下反应:
![]()
若平均每分钟生成0.5 mol的C,容器表面向外散热速率平均为400 J/(min·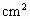 ),为了维持恒温280℃,平均每分钟需用加热器提供________kJ的热量.(简述推理过程)________.
),为了维持恒温280℃,平均每分钟需用加热器提供________kJ的热量.(简述推理过程)________.
(2)若将(1)的小型实验扩大为工业生产:将反应容器的底面半径和高度都扩大到原容器的10倍,做成“相似体”,并向其中将A、B按原比例充入,使压强仍为p,然后加热到280℃使反应开始.为了维持恒温280℃,反应开始后,应继续加热还是进行冷却?(设容器表面散热速率不变)________.
平均每分钟用加热器向体系提供或者用冷却器吸收多少千焦的热量.(简述推理过程)________.
(3)在恒温、恒压下,向(2)的“相似体”的平衡体系中,再将A、B按原比例充入,重新达到平衡时,C的体积分数为________.
(1)若平均每分钟生成0.5 mol C,容器表面向外散热速率平均为400 J·min-1·cm-2,为了维持恒温t ℃,平均每分钟需用加热器提供____________ kJ的热量。
(2)将2 mol A与1 mol B充入上述

①20 min时发生变化的条件是______________;
A.加入催化剂 B.降低温度
C.缩小了容器体积 D.增加了B物质的量
②在15 min达到平衡,此时平衡常数K=______________ (用分数表示)。若保持体系温度为t ℃,则随着反应的进行,K值____________。(填“增大”、“减小”或“不变”)
③若起始时在此
下图中A、B均为固体,其中B为单质.下图可用于工业生产F,F是衡量一个国家化工水平的标志.回答下列问题:
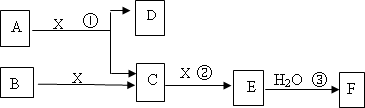
(1)A的化学式________
(2)反应①是一个氧化还原反应,该反应发生时,每生成4 mol气体C,转移电子________mol
(3)写出D与铝单质反应的化学方程式________
(4)反应②是可逆反应,在2 L的密闭容器中投入4 mol C和3 mol X,10分钟后反应达到平衡,平衡时混合气体共6 mol,则下列说法正确的是________
A.工业制取F时,C和X生成E的反应是在吸收塔进行
B.这10分钟内,X的平均速率是0.1 mol/(L·min)
C.当C和X的消耗速率比为2∶1时,标志着反应达到平衡
D.平衡时C的转化率是50%
E.在工业生产中可以通过增加X的量来提高C的转化率
F.工业生产中直接用水来吸收E
(5)写出2.24 L气体C与0.15 mol氢氧化钠溶液反应的离子化学方程式________
(6)将5 mL 0.02 mol/L的F溶液与5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的体积为10 mL,则混合液的pH是________写出F的一种用途________
1.D 2.A 3.A 4.C 5.C 6.AC 7.D 8.D 9.BD 10.AB 11.B
12.D 13.B 14.B 15.A 16.B 17.B 18.B 19.A 20.B 21.C 22.D
23.(1)< (2)右侧的3处
(3)< B相当于减压了,减压后平衡向 分解的方向移动,使B中
分解的方向移动,使B中 的量减少了.
的量减少了.
24.①提高,降低;②b=4;③ ;④
;④ 或
或 或ac+bc=ab
或ac+bc=ab
25.(1)B.根据反应:

 ,
,

 ,若要充分利用原料,显然要求原料与
,若要充分利用原料,显然要求原料与 反应产生的
反应产生的 和
和 物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用.
物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用. w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m




(2)①

 ②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中,
②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中, 抑制
抑制 的溶解,使
的溶解,使 的浓度减小,盐酸中
的浓度减小,盐酸中 抑制
抑制 的水解.
的水解.
26.(1)2、1、3、2 (2)A为气态,B为固态或气态,D为气态 (3)放热
27.(1)按1分钟计,生成0.5 mol C产生热量45 kJ,而容器散热
 ,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
(2)容器半径和高度都变为原来10倍,则表面变为原来1000倍,平均每分钟生成C为0.5 mol×1000=500 mol,放出热量45000kJ,而容器散热12000 kJ,所以冷却器每分钟吸收热量45000 kJ-12000 kJ=33000 kJ
(3)不变
28.a=1 b=2
29.(1) (2)1/10500 (3)10
(2)1/10500 (3)10
30.①39% ②12.5% 31.(1)① 体积
体积
②当活塞由C向B移动时,因体积扩大使平衡:

 向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出
向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出



起始:0.08 mol 0
平衡:

因平衡时混合气体总的物质的量为0.07 mol,由于活塞由C移至B,体积扩大,故 ,可知充入
,可知充入 物质的量必小于0.01
mol
(2)
物质的量必小于0.01
mol
(2)
 www.ks5u.com
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com