
题目列表(包括答案和解析)
2![]() +5
+5![]() +H+====2Mn2++5
+H+====2Mn2++5![]() +3H2O
+3H2O
填空回答问题:
(1)该滴定实验所需仪器有下列中的______________(填序号)。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL)
C.量筒(10 mL) D.锥形瓶
E.铁架台 F.滴定管夹
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不用___________(填写“酸”“碱”)式滴定管盛装高锰酸钾溶液,试分析原因:
____________________________。
(3)选何种指示剂,说明理由________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL。则(b-a) mL,比实际消耗KMnO4溶液体积_________(多、少),根据(b-a) mL计算,得到的待测浓度,比实际浓度________(大、小)。
现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2![]() +5
+5![]() +H+====2Mn2++5
+H+====2Mn2++5![]() +3H2O
+3H2O
填空完成问题:
(1)该滴定实验所需仪器有下列中的____________________。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL) C.量筒(10 mL) D.锥形瓶E.铁架台 F.滴定管夹 G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(2)不用____(酸、碱)式滴定管盛放高锰酸钾溶液。试分析原因:________________________。
(3)选何种指示剂,说明理由___________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积__________(多、少)。根据(b-a)mL计算得到的待测浓度,比实际浓度_____________(大、小)。
(16分)氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
⑴ 步骤Ⅰ的目的是除不溶性杂质。所需操作的名称是________、________。
⑵ 步骤Ⅱ的目的是除硫酸亚铁。操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①写出用H2O2溶液除去硫酸亚铁的离子方程式____________________________。
②调整pH 的范围应该在____________之间。
⑶ 步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是将溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。采用水浴加热的原因是____ 。
⑷ 该同学用CuSO4溶液进行如下探究实验:取A、B两支试管,分别加入 2 mL 5%H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4 溶液各1 mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因 。
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
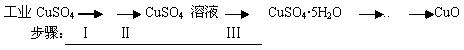
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
⑴ 步骤Ⅰ的目的是除不溶性杂质。所需操作的名称是________、________。
⑵ 步骤Ⅱ的目的是除硫酸亚铁。操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①写出用H2O2溶液除去硫酸亚铁的离子方程式____________________________。
②调整pH 的范围应该在____________之间。
⑶ 步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是将溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。采用水浴加热的原因是____ 。
⑷ 该同学用CuSO4溶液进行如下探究实验:取A、B两支试管,分别加入 2 mL 5%H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4溶液各1 mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因 。
(5)16克硫酸铜固体投入水中形成1升溶液,则该溶液显 性(填“酸性”或“碱性”或“中性”),溶液中所有阳离子总数 0.1NA(填“等于”或“大于”或“小于”),若在上述新配制溶液加入稀硫酸再加入铁片产生氢气速率会明显加快,原因是 ;室温下、若在上述新配制溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。
(16分)氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
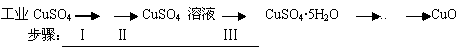
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
6.0 |
7.5 |
1.4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
⑴ 步骤Ⅰ的目的是除不溶性杂质。所需操作的名称是________、________。
⑵ 步骤Ⅱ的目的是除硫酸亚铁。操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①写出用H2O2溶液除去硫酸亚铁的离子方程式____________________________。
②调整pH 的范围应该在____________之间。
⑶ 步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是将溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。采用水浴加热的原因是____ 。
⑷ 该同学用CuSO4溶液进行如下探究实验:取A、B两支试管,分别加入 2 mL 5%H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4 溶液各1 mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因 。
1.C 2.C 3.B 4.D 5.D 6.B 7.D 8.BC 9.BC 10.CD 11.A
12.BC 13.C 14.A 15.B 16.C 17.A 18.C 19.C 20.B 21.D 22.C
23.146,即 的式量=146,求得n=5
的式量=146,求得n=5
则赖氨酸的结构简式为

生成的二肽的结构简式为

或
24.B: ;
;
D: ;
;
25.(1)

(2)

(3)
26.(1)

 CH=CHCOOH
CH=CHCOOH 
(2)氧化 消去 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
(3)解:




27.(1) (2)0.96,0.08
(2)0.96,0.08
(2)
(3)

29.解:C分子中 ,最简式为CH因C中含42个电子,故C为
,最简式为CH因C中含42个电子,故C为 ,盐B为
,盐B为
A分子中 ,∴ A为
,∴ A为
(1) (2)144 (3)
(2)144 (3)
30.解析:(1)1 mol的D与银氨溶液反应,析出 且D的组成符合
且D的组成符合 的分子式,说明该分子中有一个氧原子,且含两个醛基,则该分子应为甲醛
的分子式,说明该分子中有一个氧原子,且含两个醛基,则该分子应为甲醛 ,若D为甲醛,则C应为甲醇.
,若D为甲醛,则C应为甲醇.
(2)由题知B为不饱和酸,可与 反应,也可与
反应,也可与 反应.又∵ 0.02 mol B可与
反应.又∵ 0.02 mol B可与 反应,说明B中只含一个C=C,可设B的分子式为
反应,说明B中只含一个C=C,可设B的分子式为
(3) ,那么A应为:
,那么A应为:
又∵ 0.5 mol C可与0.5 mol B反应,而1mol A和B的混合物与0.5 mol C反应,分离出1 mol A,说明A和B的混合物中,A、B各占0.5 mol.
∴ 有0.5(12n+2n-1+12+32+15)+0.5?(12n+2n-1+12+33)=79
解之n=2
∴ B为 ,即
,即
A为
答案:
A为丙烯酸甲酯( )
)
B为丙烯酸( )
)
C为甲醇( )
)
D为甲醛(HCHO)
 w.w.w.k.s.5www.ks5u.com
w.w.w.k.s.5www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com