
题目列表(包括答案和解析)
(1)防治环境污染,改善生态环境已成为全球的共识。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质未纳入我国空气质量报告的是_______(填字母)。
a.CO2 b.SO2 c.NO2 d.可吸入颗粒物
②垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________(填字母)标志的垃圾筒内。
③工业废水需处理达标后才能排放。2012年1月15日,广西河池市龙江河发生镉污染,严重影响沿江和下游柳州市部分民众饮水,当地政府立即采用“弱碱性化学沉淀应急除镉技术”处理被污染的水体,即投放聚合氯化铝和烧碱使镉沉降。聚合氯化铝属于 。
a.消毒剂 b.混凝剂 c.氧化剂
(2)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖。
①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属元素的原子结构示意图为__________。
②铁锈的主要成分是_____________(填化学式),它是钢铁在潮湿的空气中发生______腐蚀的结果。
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有Na2CO3、______和______(填化学式)。
(3)保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段。
①人类的生命活动需要糖类、________、________、维生素、水、和无机盐(或矿物质)等六大类营养物质。
②维生素C的结构为,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
③阿司匹林具有____________作用。长期大量服用阿司匹林,其水解产物水杨酸( )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。
(1)防治环境污染,改善生态环境已成为全球的共识。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质未纳入我国空气质量报告的是_______(填字母)。
a.CO2 b.SO2 c.NO2 d.可吸入颗粒物
②垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________(填字母)标志的垃圾筒内。 
③工业废水需处理达标后才能排放。2012年1月15日,广西河池市龙江河发生镉污染,严重影响沿江和下游柳州市部分民众饮水,当地政府立即采用“弱碱性化学沉淀应急除镉技术”处理被污染的水体,即投放聚合氯化铝和烧碱使镉沉降。聚合氯化铝属于 。
a.消毒剂 b.混凝剂 c.氧化剂
(2)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖。
①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属元素的原子结构示意图为__________。
②铁锈的主要成分是_____________(填化学式),它是钢铁在潮湿的空气中发生______腐蚀的结果。
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有Na2CO3、______和______(填化学式)。
(3)保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段。
①人类的生命活动需要糖类、________、________、维生素、水、和无机盐(或矿物质)等六大类营养物质。
②维生素C的结构为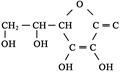 ,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
③阿司匹林具有____________作用。长期大量服用阿司匹林,其水解产物水杨酸(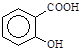 )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。
(1)防治环境污染,改善生态环境已成为全球的共识。
①空气质量报告的各项指标可以反映出各地空气的质量。下列物质未纳入我国空气质量报告的是_______(填字母)。
a.CO2 b.SO2 c.NO2 d.可吸入颗粒物
②垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________(填字母)标志的垃圾筒内。

③工业废水需处理达标后才能排放。2012年1月15日,广西河池市龙江河发生镉污染,严重影响沿江和下游柳州市部分民众饮水,当地政府立即采用“弱碱性化学沉淀应急除镉技术”处理被污染的水体,即投放聚合氯化铝和烧碱使镉沉降。聚合氯化铝属于 。
a.消毒剂 b.混凝剂 c.氧化剂
(2)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖。
①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属元素的原子结构示意图为__________。
②铁锈的主要成分是_____________(填化学式),它是钢铁在潮湿的空气中发生______腐蚀的结果。
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有Na2CO3、______和______(填化学式)。
(3)保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段。
①人类的生命活动需要糖类、________、________、维生素、水、和无机盐(或矿物质)等六大类营养物质。
②维生素C的结构为 ,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
③阿司匹林具有____________作用。长期大量服用阿司匹林,其水解产物水杨酸( )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式:
。
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式:
。

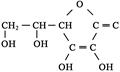 ,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。
,它是一种水溶性的维生素,缺乏VC会使人患上坏血病。切取一片新鲜水果,向切面上滴加淀粉和碘水的混合溶液,会发现混合溶液蓝色褪去,这说明新鲜水果中的VC具有____________(填“氧化”或“还原”)性质。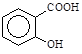 )可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。
)可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解。写出水杨酸与小苏打反应的化学方程式: 。汞(Hg)、铬(Cr)是影响环境污染、生物效应和人类健康的重金属元素。
I、铬广泛应用于钢铁工业、磁带和录像带等方面。
(1)工业常采用“铝在高温条件下还原铬绿(Cr2O3)”制备铬单质,该反应的化学方程式为 。
II、含铬的工业废水会导致慢性中毒。处理含+6价铬的废水时可得到铁氧体(其组成可写作[Fe2+Fe3+(2-x) Cr3+x]O4)。

(2)加过量FeSO4的目的是 。
(3)配平步骤①的反应的离子方程式 Fe2++ Cr2O72—+ _____== Fe3++ Cr3++ H2O
并计算铁氧体( [Fe2+Fe3+(2-x) Cr3+x]O4)中X= _________________。
(4)下表是实验检测中心对某地区二个点的土壤样品(每个点分三层取样,共6个样品)进行了有机质和铬总量的测定,结果见下表。
|
样品序号 |
取样深度(m) |
有机质(×10—2g) |
总铬(×10—6g) |
|
样品A-1 |
0.00 ~ 0.30 |
2.81 |
114 |
|
样品A-2 |
0.30 ~ 0.60 |
1.72 |
111 |
|
样品A-3 |
1.20 ~ 1.80 |
1.00 |
88 |
|
样品B-1 |
0.00 ~ 0.30 |
2.60 |
116 |
|
样品B-2 |
0.30 ~ 0.60 |
2.48 |
112 |
|
样品B-3 |
1.20 ~ 1.80 |
1.83 |
106 |
从表中你可以得出的结论有 (答一点即可)。
(5)工业上以铬酸钾(K2CrO4)为原料,电化学法制备重铬酸钾,装置如图。反应为:4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+
2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为
。原因是
。
Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为
。原因是
。

1.D 2.C 3.C 4.B 5.C 6.C 7.BC 8.BD 9.AC 10.D 11.C
12.BD 13.AC 14.A 15.B 16.D 17.B 18.D 19.B 20.D
21.D 22.C w.w.w.k.s.5.u.c.o.m
23.(1)促进,A (2)甲大
乙用氯化铵溶液稀释后,[ ]增大很多,使
]增大很多,使 的电离平衡向抑制电离的方向移动;
的电离平衡向抑制电离的方向移动; 发生水解,使稀释后的乙溶液的[
发生水解,使稀释后的乙溶液的[ ]增大
]增大
24.(1)第一种组合 A:NaOH B:
第二种组合 A: B:
B:
(2)由于 电离出
电离出 ,使水的电离平衡:
,使水的电离平衡:

 向左移动,使水的电离度小于纯水中水的电离度,而
向左移动,使水的电离度小于纯水中水的电离度,而 溶液中由于
溶液中由于


由于 电离出的
电离出的 与
与 结合生成弱电解质
结合生成弱电解质 ,从而促进水的电离,使水的电离度比纯水中的大.
,从而促进水的电离,使水的电离度比纯水中的大.
25.(1)偏高;空气中的氧气溶于样品中
(2)偏高;使 溶液浓度变低,消耗体积偏大
溶液浓度变低,消耗体积偏大
(3)偏高;使最后读取体积数比实际消耗 溶液体积数大
溶液体积数大
(4)
26.(1)增大w.w.w.k.s.5.u.c.o.m
(2)K值越大,酸性越强
(3)

(4) 上一级电离产生的
上一级电离产生的 对下一级电离有抑制作用
对下一级电离有抑制作用
(5)
27.(1) 和
和 水解均呈弱酸性,可除去金属表面的氧化物
水解均呈弱酸性,可除去金属表面的氧化物
(2) 水溶液中[
水溶液中[ ]很小,不会生成沉淀(或弱酸不能生成强酸).加入氨水时,
]很小,不会生成沉淀(或弱酸不能生成强酸).加入氨水时,

 ,使
,使 电离平衡右移,[
电离平衡右移,[ ]增大,产生沉淀(或
]增大,产生沉淀(或 与
与 生成
生成 ,使[
,使[ ]增大
]增大
(3)在HCl气流中, 抑制
抑制 水解,从而可得到
水解,从而可得到 无水物
无水物
(4)能. ,降低[
,降低[ ],其水解平衡左移,碱性减弱
],其水解平衡左移,碱性减弱
(5) 水解呈碱性,
水解呈碱性, 水解呈酸性,二者混合施用,会促进水解,大量生成易挥发的
水解呈酸性,二者混合施用,会促进水解,大量生成易挥发的 ,从而使氮肥降低肥效
,从而使氮肥降低肥效
 电离呈酸性,与
电离呈酸性,与 混合施用,会产生
混合施用,会产生 或
或 沉淀而丧失肥效.
沉淀而丧失肥效.
硫铵(即硫酸铵)水解呈酸性,长期施用土壤会板结酸化,加消石灰可调节酸度,防止板结.
28.(1)造成测定数值偏高w.w.w.k.s.5.u.c.o.m
(2)
(3)
29.(1) ;
; 、
、
(2)1.90 2.67 5.20
(3)130
分析:(1)因为在浊液中加入HCl溶液至10 mL,沉淀质量一直为 形式存在,继续加入HCl溶液,
形式存在,继续加入HCl溶液, 转变为
转变为 沉淀,加至30 mL时,
沉淀,加至30 mL时, 全部转变为
全部转变为 ,所以在A点的沉淀物为
,所以在A点的沉淀物为 ,在A至B点间,沉淀物为
,在A至B点间,沉淀物为 和
和 的混合物.当加入的HCl溶液超过30 mL时,
的混合物.当加入的HCl溶液超过30 mL时, 和
和 同时溶解.w.w.w.k.s.5.u.c.o.m
同时溶解.w.w.w.k.s.5.u.c.o.m
(2)原混合物中:
 的质量
的质量


 的质量
的质量
NaOH:
①浊液中存在的:
1×0.01 mol
② 消耗的:
消耗的:


③ 消耗的:
消耗的:

0.02 mol×4=0.08 mol
NaOH总质量
(3)从B点开始, 消耗的HCl:0.02 mol×3=0.06 mol
消耗的HCl:0.02 mol×3=0.06 mol
 消耗的HCl:0.02 mol×2=0.04 mol
消耗的HCl:0.02 mol×2=0.04 mol
所消耗HCl溶液的体积为:
Q点HCl溶液总量为:30 mL+100 mL=130 mL
30.(1)
(2)

根据 
过量 为:
为:
20.00 mL水样消耗 为
为
根据得电子数目相等,则有
相当于 为:
为:
 ,即该水样的
,即该水样的
(3)
(4)A,
 www.ks5u.com
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com