
题目列表(包括答案和解析)
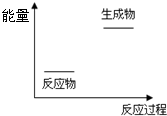 关于化学反应与能量的说法正确的是( )
关于化学反应与能量的说法正确的是( )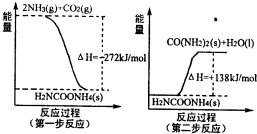
| 温度/ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
2- 3 |
- 3 |
2- 3 |
- 3 |
- 3 |
2- 3 |
2- 3 |
- 3 |
从能量的变化和反应的快慢等角度研究反应: 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A.使用催化剂 B.适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是________。
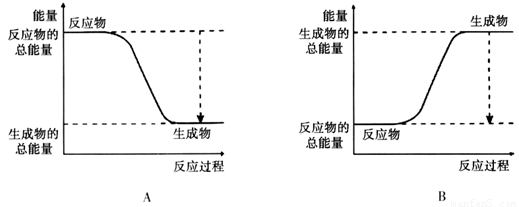
(3)从断键和成键的角度分析上述反应中能量的变化。
【资料】①键能:拆开1mol化学键需要吸收的能量,或是形成1mol化学键所放出的能量称为键能。
②化学键的键能:
|
化学键 |
H—H |
O=O |
H—O |
|
键能 |
436 |
496 |
463 |
请填写下表:
|
化学键 |
填“吸收热量” 或“放出热量” |
能量变化 |
|
|
拆开化学键 |
|
_______________ |
_______________ |
|
|
|||
|
形成化学键 |
|
_______________ |
_______________ |
|
总能量变化 |
_______________ |
_______________ |
(4)氢氧燃料电池的总反应方程式为 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
在化学反应中,反应物转化成生成物,必然发生能量的变化。
(1)下列说法正确的是 。
| A.化学变化中的能量变化主要由化学键变化引起的 |
| B.放热反应发生时不一定要加热,但吸热反应必须要加热才能发生 |
| C.钢铁的吸氧腐蚀和析氢腐蚀的负极反应都为Fe—2e一= Fe2+ |
| D.CaCO3(s) =" CaO(s)" + CO2(g) ΔH=" +" 178.5 KJ·mol-1的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量 |
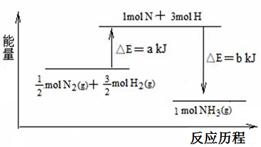
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷。
第Ⅰ卷共18小题,每题6分.共108分。
一、选择题:选对的给6分,选错的或未选得给0分。
1.C 2.D 3.A 4.A 5.B 6.D 7.C 8.B 9.C 10.D 11.B 12.C
二、选择题:全部选对的给6分,选对但不全的给3分,有选错得或未选的给0分。
13.C 14.A、D 15.D 16.B 17.A、D 18.D
%20理科综合(一).files/image096.jpg)
第Ⅱ卷必考部分共9题,共157分。
19.(18分)
(1)1.996~1.998 (2分) 1.094(2分)
(2)保护电源,防止短路(2分)
(3)如右图所示(有一处错就不给分)(4分)
(4)2.9;1.0(4分)
(5)多测几组R、U,分别求出电动势E、内阻r,再求E、r的平均值(2分);
或利用U-I图象处理数据。(2分)
20.(15分)
解:(1)解除锁定弹开物块AB后,两物体的速度大小
%20理科综合(一).files/image098.gif) ①(2分)
①(2分)
弹簧储存的弹性势能%20理科综合(一).files/image100.gif) ②(3分)
②(3分)
(2)物块B滑上传送带匀减速运动,当速度减为零时,滑动的距离最远.
由动能定理得:%20理科综合(一).files/image102.gif) ③(2分)
③(2分)
得:%20理科综合(一).files/image104.gif) ④(2分)
④(2分)
(3)物块B沿传送带向左返回时,先匀加速运动,物块速度与传送带速度相同时再一起匀速运动,设物块B加速到传送带速度v需要滑动的距离为%20理科综合(一).files/image106.gif)
由%20理科综合(一).files/image108.gif) 得
得%20理科综合(一).files/image110.gif)
%20理科综合(一).files/image112.gif) ⑤(3分)
⑤(3分)
表明物块B滑回水平面MN的速度没有达到传送带的速度
所以: %20理科综合(一).files/image114.gif) ⑥(3分)
⑥(3分)
21.(19分)
解:(1)输电线冰层的体积V冰 = πR2L (2分)
由对称关系可知,塔尖所受压力的增加值等于一根导线上冰层的重力,即
%20理科综合(一).files/image115.gif) Δm = ρV冰 g= πρR2Lg (2分)
Δm = ρV冰 g= πρR2Lg (2分)
(画出受力图示正确给4分)
(2)输电线与冰层的总质量M' = m0L + πρR2Lg,(1分)
输电线受力如图甲所示。
由共点力的平衡条件,得2F1cosθ = m0Lg + πρR2Lg (3分)
输电线在最高点所受的拉力%20理科综合(一).files/image117.gif) (2分)
(2分)
半根输电线的受力如图乙所示。
由共点力的平衡条件,得F2 = F1sinθ (3分)
输电线在最低点所受的拉力%20理科综合(一).files/image119.gif) (2分)
(2分)
22.(20分)
解:(1)电场力与洛伦兹力平衡得:qE=qv0B得:E=v0B 方向竖直向上 (2分)
(2)根据运动的对称性,微粒能从P点到达Q点,应满足%20理科综合(一).files/image121.gif) (2分)
(2分)
其中x为每次偏转圆弧对应的弦长,偏转圆弧对应的圆心角为%20理科综合(一).files/image123.gif) 或
或%20理科综合(一).files/image125.gif) . (2分)
. (2分)
设圆弧的半径为R,则有2R2=x2,可得:%20理科综合(一).files/image127.gif) (2分)
(2分)
又%20理科综合(一).files/image129.gif) 由①②③式得:
由①②③式得:%20理科综合(一).files/image131.gif) ,n=1、2、3、……
(2分)
,n=1、2、3、……
(2分)
(3)当n取奇数时,微粒从P到Q过程中圆心角的总和为
%20理科综合(一).files/image133.gif) ,(2分)
,(2分)%20理科综合(一).files/image135.gif) ,其中n=1、3、5、…(2分)
,其中n=1、3、5、…(2分)
当n取偶数时,微粒从P到Q过程中圆心角的总和为:
%20理科综合(一).files/image137.gif) ,(2分)
,(2分)%20理科综合(一).files/image139.gif) ,其中n=2、4、6、……(2分)
,其中n=2、4、6、……(2分)
%20理科综合(一).files/image140.gif) 欲使时间最小,取n=1或者2,此时
欲使时间最小,取n=1或者2,此时%20理科综合(一).files/image142.gif) (2分)
(2分)
23.(15分)
%20理科综合(一).files/image144.jpg) 解:(1)H (1分)
(2) (1分)
解:(1)H (1分)
(2) (1分)
(3)3Cu + 2NO3- + 8H+ === 3Cu2+ + 2NO↑ + 4H2O(3分)
%20理科综合(一).files/image146.gif) (4)①
NH4+ + OH- H2O +
NH3 ↑ (2分)
(4)①
NH4+ + OH- H2O +
NH3 ↑ (2分)
② SO32- + Cl2 + H2O = SO42- + 2Cl- + 2H+ (3分)
(5)① (NH4)2Fe(SO4)2?6H2O (2分)
② 5Fe2+ + MnO4- + 8H+ = 5Fe3++ Mn2+ + 4H2O (3分)
24.(15分)
解:⑴2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O(2分)
|