
题目列表(包括答案和解析)
| 部分钙、镁化合物溶解性表(20℃) | |||
| 阴离子阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入 Na2CO3溶液. | 没有白色沉淀产生 | ______ |
| 部分钙、镁化合物溶解性表(20℃) | |||
| 阴离子阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入 Na2CO3溶液. | 没有白色沉淀产生 | ______ |
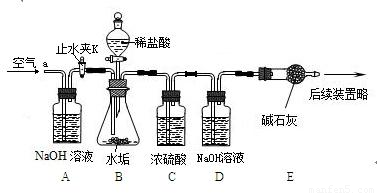
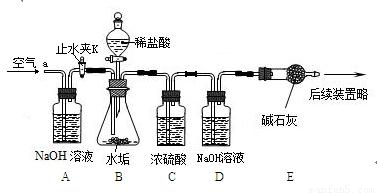
 在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.
在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.| 实验步骤 | 实验现象 | 解释、结论 |
| 取少量溶液,向溶液中加入 过量 过量 (填“少量”或“过量”)的CaCl2溶液,过滤. |
现象: 出现白色沉淀 出现白色沉淀 |
反应的化学方程式为 CaCl2+Na2CO3=CaCO3↓+2NaCl CaCl2+Na2CO3=CaCO3↓+2NaCl |
| 取上述实验所得溶液少量,滴加3滴酚酞试剂. | 现象: 溶液变红 溶液变红 |
结论:C |
 21、化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
21、化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
说明:1.本试卷有多题的答案是开放的,若考生写出其他合理答案,应参照此意见给分。
2.本卷每个化学方程式都是1分。化学式错误的不给分;未配平、未写反应条件、未标出
“↑”“↓”应扣0.5分,但每个化学方程式最多扣0.5分。
一、选择题(本大题包括15小题,其中第1―10题每小题1分,第11―15每小题2分,共20分)
每小题只有一个选项符合题意。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
D
D
B
A
B
A
C
B
D
B
B
C
C
C
B
二、填空题(本大题包括4小题,每空1分,共17分)
16.(4分) (1)酸H2CO3;(2)碱 Ca(OH)2 ;(3)盐 CaCO3或Ca(HCO3)2 ;
(4)氧化物H20
17.(4分) (1)____1___;(2)____2____;(3) __5____;(4) _4_____。
18.(4分)
(1)__CaO+H2O=Ca(OH)2_________ ;
(2) Na2CO3+ Ca(OH)2_ =CaCO3↓+2NaOH ;
(3) Na2CO3+2HCl=NaCl+ H2O+CO2 ↑ ;
(4) Fe + CuSO4 =Cu + FeSO4 ______ 。
19.(5分) (1) Na2CO3 Na2SO4 BaCl2 ;CuSO4;KNO3 、 NaCl 。(填化学式)
(2)Na2CO3+ BaCl2 =BaCO3+ NaCl; Na2SO4+ BaCl2= BaSO4↓+ 2NaCl 。
三、实验题(本大题包括3小题,每空1分,共17分)
20.(5分)(1) 物理 过滤 (2) 蛋白质、脂肪、糖类 Fe (3) B D
21、(5分)(1)溶液中H+使CuO溶解。(2) H2O不能溶解CuO。(3) 盐酸或硫酸钠溶液
(4)溶液中的H+可以使CuO溶解,H2O SO42-不能使CuO溶解;稀HNO3或HCl
22.(7分)(1)都是一个密闭的体系里设法消耗CO2,使得气体压强减少,从而观察到明显现象;
CO2能溶于水,究竟是CO2溶于水使气压减小的结果?还是CO2与NaOH反应使气压减小的结果?;
做个对比实验:取一个与甲装置同样大小的软塑料瓶,充满CO2后,注入与氢氧化钠溶液体积相同的水,振荡,比较瓶子变瘪的程度,即可判断。
(2)
实验步骤和方法
实验现象
实验结论
方案1

①产生气泡
CO2和NaOH确实发生了化学反应
方案2
②将CO2通入NaOH溶液后,再滴加CaCl2溶液(或石灰水或BaCl2溶液或Ba(OH)2溶液)其他答案也可以
③出现白色浑浊(或产生白色沉淀)
CO2+2NaOH=Na2CO3 +H2O , Na2CO3 +CaCl2=CaCO3↓+2NaCl
四、计算题(本大题包括1小题,共6分)
23.(6分)
(1)0.
|