
题目列表(包括答案和解析)
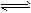 2CO(g) (正反应吸热),升高温度会加快化学反应速率
2CO(g) (正反应吸热),升高温度会加快化学反应速率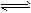 PCl3(g)+Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小
PCl3(g)+Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小 | A.对于反应C(s)+CO2 (g)=2CO(g)△H>0,升高温度会加快化学反应速率 |
| B.将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 |
| C.合成氨反应中,当3v(NH3)正=2v(H2)逆时,反应达到平衡 |
| D.对于反应PCl5(g)?PCl3(g)+Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小 |
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
(1)已知:N2(g)+ O2(g)=2NO(g)△H=+180.5 kJ/mol
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393.5kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H= 。
(2)某研究性学习小组在技术人员的指导下,在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①前2s内的平均反应速率v (N2) = ___________________。
②在该温度下,反应的平衡常数K = 。(只写出计算结果)
③对于该可逆反应,通过综合分析以上信息,至少可以说明 (填字母)。
A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应体系达到平衡时至少有一种反应物的百分含量较小
D.该反应在一定条件下能自发进行
E.该反应使用催化剂意义不大
(3)CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是 。
A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
说明:1. 文字简答题以关键词到位为准,按点给分;
2. 化学用语书写:(1)方程式未配平不得分、无条件扣一半分值;
(2)化学式书写错误得0分;
3. 写名称或化学式正确的正常给分; 4. 其他合理解法正常给分。
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意。)
二、选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
A
C
B
D
A
B
D
B
AC
C
A
BD
D
AD
第Ⅱ卷(非选择题 共72分)
三、(本题包括1小题,共10分)
15.(10分)(1)NH4[CuCl2] =CuCl↓+NH4Cl(1分),避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分(1分)。(2)蒸馏(1分),NH4Cl、HNO3(2分)。 (3) B(2分) (4)氯化铵溶于水吸收大量热量,造成反应液温度降低(1分)。 烧瓶上方红棕色气体逐渐变为无色(1分),a或c(1分)(答a或答c给分)
四、(本题包括2小题,共18分)
16.(8分)(1)六 ⅣA (各1分,共2分)(2)不变(2分)
(3) Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O (2分)
(4)Na2S2O3标准溶液浓度和滴定溶液体积(2分)
17.(10分)(1)CH4+H2O
 CO+3H2(2分)(2)n (2分)(3)Fe2O3?H2O(2分)
CO+3H2(2分)(2)n (2分)(3)Fe2O3?H2O(2分)
 |
(4) 优点是:NaOH可以循环利用,同时获得副产品氢气。(各2分,共4分,优点答到“NaOH可以循环利用”即可)
五、(本题包括1小题,共10分)
18.(10分)(1)氯化铵(2分)
(2)原因是降低KH2PO4溶解度,使其析出后,降低了生成物浓度,(同时生成的HCl与三正丁胺反应,也降低了HCl的浓度),使平衡向正反应方向移动。(2分,答到一点即可)。分离出氯化氢(2分,其他合理答案均给分)(3)50―60均可,95%(填近似值即可)(各2分,共4分)
六、(本题包括1小题,共12分)
19.(12分)(1)与生成的硫酸反应,促进平衡向正反应方向移动。(2分)
(2) (2分)
(2分)
(3)2(1分)
(4) (2分)
(2分)
(5)保护A中的酚羟基。(2分)
(6)(3分,第一步正确得2分,完全正确得3分)

|