
题目列表(包括答案和解析)
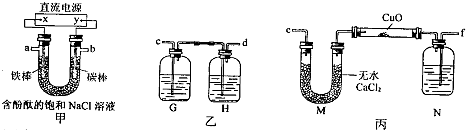
某化学兴趣小组拟采用下图所示装置电解饱和氯化钠溶液制备H2,通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),同时检验Cl2的氧化性(图中夹持和加热仪器已略去)。
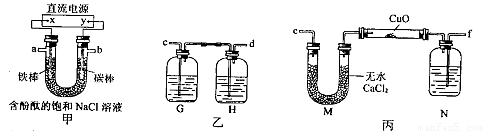
(1)直流电源中的X极为 极(填“正”、“负”、“阴”或“阳”);写出甲装置U形管中反应的离子方程式: ;实验开始后,用铁棒作电极的一侧的实验现象是 。
(2)为完成上述实验,正确的链接顺序为:a连 ,b连 (填写连接的字母)。
(3)装置乙中的G瓶内溶液可能为 (填字母)。
A.淀粉KI溶液 B.NaOH溶液 C.Na2S溶液 D.Na2SO3溶液
H瓶内的反应的离子方程式为: 。
(4)在对硬质玻璃试管里的氧化铜粉末加热前需要进行的操作为: 。
(5)装置丙中N瓶内盛放的试剂为 ,作用是 。
(6)为了测定Cu的相对原子质量,某同学通过实验测得如一下数据:
I.氧化铜样品质量为m1g
Ⅱ.反应后硬质玻璃管中剩余固体质量为m2g
Ⅲ.反应前后U形管及其固体质量差为m3g
Ⅳ.反应前后瓶及其液体质量差为m4g
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)= 。
②如果选用其它数据进行计算,会导致Ar(Cu) (填“偏大”、“偏小”或“无影响”),理由是 。
某化学兴趣小组拟采用下图所示装置电解饱和氯化钠溶液制备H2,通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),同时检验Cl2的氧化性(图中夹持和加热仪器已略去)。
(1)直流电源中的X极为 极(填“正”、“负”、“阴”或“阳”);写出甲装置U形管中反应的离子方程式: ;实验开始后,用铁棒作电极的一侧的实验现象是 。
(2)为完成上述实验,正确的链接顺序为:a连 ,b连 (填写连接的字母)。
(3)装置乙中的G瓶内溶液可能为 (填字母)。
| A.淀粉KI溶液 | B.NaOH溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
| A.淀粉KI溶液 | B.NaOH溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
 为探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组设计了如右图所示的实验装置.试填空.
为探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组设计了如右图所示的实验装置.试填空.


1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A
B
D
C
C
B
C
D
D
C
C
B
B
A
D
16.每空2分,共8分。
(1)2ClO3-+SO2 ===2ClO2+SO42-;(2)D;(3)4.816a×1023;(4)8┱1。
17.共10分。
⑴D(1分);⑵Cu(1分);H2(1分);⑶①随着反应进行生成铝离子浓度增大,水解产生的H+的浓度增大,②该反应放热,升高温度反应加快,③铜与铝构成原电池,加快铝溶解;(3分)⑷A、B、D;(2分,少选、错选均不给分)⑸A(1分),电解质性质(1分)(其它合理解答同样给分)。
 18.共10分。
18.共10分。
⑴Na (1分) ;⑵ Cl―<S2―(1分)
⑶极性共价键(1分),非极性分子(1分);NH3(1分);c、d (1分,少选、错选均不给分) ;⑷H2S+Cl2=2HCl+S↓(2分);⑸Cl2(1分), 原子晶体(1分)。
19.每个方程式2分,其它每空1分,共8分。
⑴ade(1分,少选、错选均不给分);⑵FeCl3(1分);防止氯化亚铁被氧化(1分);Fe3++3SCN-=Fe(SCN)3(2分,合理反应都可以给分);⑶Al(OH)3(1分);Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)。
20.每空1分,共11分。
【方法一】⑴分液漏斗;浓硫酸;防止外界水蒸气进入;⑵87.4% ;SO2不能完全被吸收 ,装置中有SO2滞留。
【方法二】2Na2SO3+O2=2Na2SO4
;[(
【方法三】(1)不能;酸性条件下Ba(NO3)2将SO2氧化成BaSO4;(2) 向漏斗内加水至刚好浸没沉淀,待水自然流出后再加水洗涤2~3次。
21.每空2分,共8分。
⑴3Cu2O+14H+ +2NO3- =6Cu2+ +2NO↑+7H2O;⑵32g;⑶0.2mol;⑷0.1<n<0.3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com