
题目列表(包括答案和解析)
)写出下列反应的离子方程式:
(1)氢氧化钠与硫酸反应 ;
(2)实验室制取CO2气体 ;
(3)少量CO2气体通入澄清石灰水 ;
(4)硫酸铜溶液与氢氧化钠反应 。
)由若干种可溶性物质组成的固体混合物X,可能含有的阳、阴离子分别是:
| 阳离子 | Na+、Mg2+ 、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、SO42-、SO32—、CO32- |
为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
(1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是__________________。
(2)向溶液中滴加盐酸溶液。刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则X中一定存在的离子是____________________,一定不存在的离子有____________________。
(3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可)____________。
(4)尚待检验的离子及检验方法是:
| 尚待检验的离子 | 检验方法 |
Ⅰ)⑴已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=-483.6kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的△H= ▲ 。
2NH3(g)的△H= ▲ 。
⑵在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ▲ ;
②达到平衡时NH3的体积分数为 ▲ 。
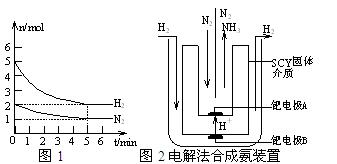
⑶近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 ▲ 。
Ⅱ)甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20molCH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。

(1)温度不变,缩小体积,增大压强,①的反应速率 ▲ (填“增大”、“减小”或“不变”),平衡向 ▲ 方向移动。
(2)反应①的△H1 ▲ 0(填“<”、“=”或“>”)。
)写出下列物质在水溶液里的电离方程式:
(1)硫酸铁 ;
(2)氢氧化铝 ;
(3)硫酸氢钾 。
(6分))有一瓶澄清溶液, 可能含有大量H+、NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO![]() 、CO
、CO![]() 、NO
、NO![]() 、Cl-、I-,现进行如下实验:
、Cl-、I-,现进行如下实验:
(1)测知溶液显强酸性;
(2)取样加少量四氯化碳和数滴新制氯水、CCl4层为紫红色;
(3)另取样滴加稀NaOH溶液, 使溶液变为碱性, 此过程无沉淀生成;
(4)取少量上述碱性溶液, 加Na2CO3溶液出现白色沉淀;
(5)将实验(3)中的碱性溶液加热, 有气体放出,该气体能使湿红色石蕊试纸变蓝。
由此可以推断:
溶液中肯定存在的离子有 ;
溶液中肯定不存在的离子有 ;
溶液中不能确定是否存在的离子有 。
题号
1
2
3
4
 5
5
6
7
8
9
答案
D
C
C
A
D
B
BC
C
B
题号
10
11
12
 13
13
14
15
16
17
18
答案
AD
C
A
B
B
B
A
D
B
19.(9分)
(1)A MnO2 浓盐酸 B 饱和食盐水 D NaOH溶液
(2)分液漏斗
(3)2NaBr+Cl2=2NaCl+Br2
(4)90%
20.(8分)
(1)B
(2)① 过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量,并且过氧化钠为粉末状不易全部转移到锥形瓶中。
(3)A 偏大
(4)
21.(6分)
(1)2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
(2)Ca(ClO)2
(3)Ca(ClO)2 + CO2 + H2O == CaCO3↓+ 2 HClO
(4)碱性
 22.(8分)(1)B:Na2O2 E:NaHCO3;
22.(8分)(1)B:Na2O2 E:NaHCO3;
(2)2Na+2H2O=2NaOH+H2↑。
(3)CO2+2OH-=CO32-+H2O。
(4)2NaHCO3+2Na2O2 2Na2CO3+2NaOH+O2↑。
2Na2CO3+2NaOH+O2↑。
23.(11分)
(1)A.HCl(或浓HCl) C.Cl2 D.KBr G.KI
(2)C+D:Cl2+2KBr=2KCl+Br2 ;A+B:4HCl+MnO2 MnCl2+Cl2↑+2H2O;②;C
MnCl2+Cl2↑+2H2O;②;C
(3)5:1
24.(5分)(1)2Fe2++Cl2=2Fe3++2Cl-; (2)2x=3n; (3)x>;(4)1.5n。
25.(6分)(1)
26.(6分)(1)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com