
题目列表(包括答案和解析)
(1)
已知:N2(g)+O2(g)=2NO(g);ΔH=+180.5 kJ·mol-14NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g):ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的
2NH3(g)的
(2)在一定条件下,将2 mol N2与5 mol H2混合于一个10 L的密闭容器中,反应情况如图所示:

①求5 min内的平均反应速率v(NH3)________;
②达到平衡时NH3的体积分数为________.
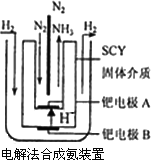
(3)近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图).钯电极A上发生的电极反应式是________.
(1)已知:N2(g)+O2(g)===2NO(g);ΔH=180.5 kJ·mol-1
4NH3(g)+5O2(g)===4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的ΔH=______________。
2NH3(g)的ΔH=______________。
(2) 甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应过程 | 化学方程式 | 焓变△H(kJ/mol) | 活化能Ea(kJ/mol) |
甲烷氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
蒸汽重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
回答下列问题:
反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H= kJ/mol
(3) 如图所示装置可用于制备N2O5,则N2O5在电解池的______(填“阳极”或“阴极”)区生成,其电极反应式为______________________________。

| |||||||||||||||||||||||||||||
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
⑴已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H= ▲ 。
⑵某研究性学习小组在技术人员的指导下,按下列流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。
![]()
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、 ▲ 等必须相同。
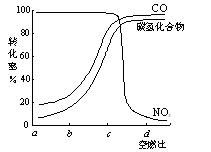
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。
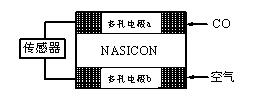
⑶CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。
下列说法错误的是 ▲ 。
A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
⑴已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol
C(s)+ O2(g)=CO2(g) △H=-393.5kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H= ▲ 。
⑵某研究性学习小组在技术人员的指导下,按下列流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。
![]()
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、 ▲ 等必须相同。
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。
⑶CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。
下列说法错误的是 ▲ 。
A.负极的电极反应式为:CO+O2—―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
一、单项选择题(本题包括8小题,每题3分,共24分。)
1.D 2.A 3.B 4.C 5.A 6.D 7.C 8.B
二、不定项选择题(本题包括6小题,每小题4分,共24分。)
9.AB 10.A 11.CD 12.BD 13.BC 14.D
三、非选择题(本题包括6小题,共60分)
15.(10分)
⑴ 将奶粉中氮元素全部转变为NH4+ 使反应中生成的氨气全部进入吸收液
⑵ 防止倒吸
⑶ 13.6
⑷ 无法确定氮元素是否一定来自于蛋白质
16.(8分)
|