
题目列表(包括答案和解析)
 (1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注.甲醛是室内主要空气污染物之一(其沸点是-19.5
(1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注.甲醛是室内主要空气污染物之一(其沸点是-19.5 (1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注.甲醛(CH2O)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因是
(1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注.甲醛(CH2O)是室内主要空气污染物之一(其沸点是-19.5℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高于甲醛的主要原因是

(1)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和
食品安全也越来越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是―19.5
℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65℃),甲醇的沸点明显高
于甲醛的主要原因是 ;甲醛分子中C的杂化方式为 ,分
子中共有 个π键。
(2)砷化镓属于第三代半导体,它能直接将电能转化为光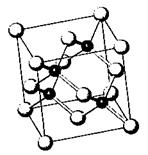 能。已知砷化镓的晶胞结构如
能。已知砷化镓的晶胞结构如
右图。是回答下列问题:
① 下列说法正确的是 (选填序号)
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
② Ga的核外电子排布式为 ;
③ 砷化镓是将(CH3) 3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,
反应的方程式为 ;(CH3) 3Ga中碳镓键之间键角为 。
一、单项选择题(本题包括8小题,每题3分,共24分。)
1.D 2.A 3.B 4.C 5.A 6.D 7.C 8.B
二、不定项选择题(本题包括6小题,每小题4分,共24分。)
9.AB 10.A 11.CD 12.BD 13.BC 14.D
三、非选择题(本题包括6小题,共60分)
15.(10分)
⑴ 将奶粉中氮元素全部转变为NH4+ 使反应中生成的氨气全部进入吸收液
⑵ 防止倒吸
⑶ 13.6
⑷ 无法确定氮元素是否一定来自于蛋白质
16.(8分)
|