
题目列表(包括答案和解析)
(11分)硫酸亚铁铵的化学式为(NH4)2SO4•FeSO4•6H2O,商品名为莫尔盐。可由硫酸亚铁与硫酸铵反应生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
(NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
(NH4)2SO4•FeSO4•6H2O | 17.2 | 26.4 | 33.0 | 46.0 | ― | ― |
(一)实验室制取少量莫尔盐的流程如下:
 |
试回答下列问题:
(1)步骤1中加入10%Na2CO3溶液的主要作用是除去铁屑表面的油污,简述其除去油污的原理
(2)将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机
(3)步骤4中析出的晶体不含(NH4)2SO4和FeSO4的原因是 ,理论上制得的莫尔盐的质量为 。
(二)称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的KMnO4酸性溶液进行滴定。
(1)滴定时,将KMnO4酸性溶液装在_______(填“酸式”或“碱式”)滴定管。试写出该滴定过程中的离子方程式:_ ___ __;
(2)判断该反应到达滴定终点的现象为 ;
(3)假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为 mol/L
(8分)亚铁盐在空气中易被氧化,但形成复盐可稳定存在。硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]是一种重要化学试剂,实验室可用纯铁片来制取硫酸亚铁铵,流程如下:

请回答下列问题:
(1)操作Ⅰ的名称是 ,所用主要仪器和用品有(铁架台、铁圈除外)
。
(2)若A物质为CuSO4,其加入的目的是 ,则固体B的成分为 。
(3)加少量硫酸可以调节pH为 1~2,其作用是 。
亚铁盐中,FeSO4•7H2O露置于空气中易被氧气氧化,而莫尔盐[(NH4)2SO4•FeSO4•6H2O]露置于空气中不易被氧气氧化,是一种重要的定量分析试剂。其制备原理是:FeSO4+(NH4)2SO4+6H2O =(NH4)2SO4•FeSO4•6H2O。
实验室用废铁屑制备莫尔盐的过程如下:

(1)步骤I除锈的操作是:将废铁屑放入烧杯, ,过滤,洗涤。
(2)步骤II铁屑的溶解在锥形瓶中进行,并水浴加热到60℃左右,需要的仪器是铁架台、石棉网、大烧杯、 。
(3)步骤III中加入的(NH4)2SO4与溶液中FeSO4的物质的量需满足的关系为:n[(NH4)2SO4]∶n[FeSO4]= 。
为了确定(NH4)2SO4的用量,下列方法简便可行的是 (填编号)。
A.称量废铁屑的质量,推算所需(NH4)2SO4的质量
B.称量无锈铁屑和步骤II之后剩余铁屑的质量,推算所需(NH4)2SO4的质量
C.测定FeSO4溶液的浓度和体积,推算所需(NH4)2SO4的质量
(4)所得晶体样品中可能混有的杂质是FeSO4·7H2O和(NH4)2SO4中的一种。某小组 设计了如下方案进行检验和测定,请在答题卡上完成表中内容。
|
序号 |
实验方案 |
实验现象和结论 |
|
步骤1 |
取少量样品 |
样品颜色可能有变化。 |
|
步骤2 |
步骤1后将样品转移到试管中,加入去氧蒸馏水,振荡溶解,调节至酸性,________ ___________ __ 。 |
若 ,说明样品中含有FeSO4·7H2O杂质。 |
|
步骤3 |
若步骤2证明样品不含FeSO4•7H2O杂质,再另取样品测定其中NH4+的质量分数w1与理论值w2比较。 |
若w1 w2,说明样品中含有(NH4)2SO4杂质。 |
(已知(NH4)2SO4•FeSO4•6H2O的式量为392,(NH4)2SO4的式量为132)
(12分)硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O是一种重要化学试剂,实验室用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:
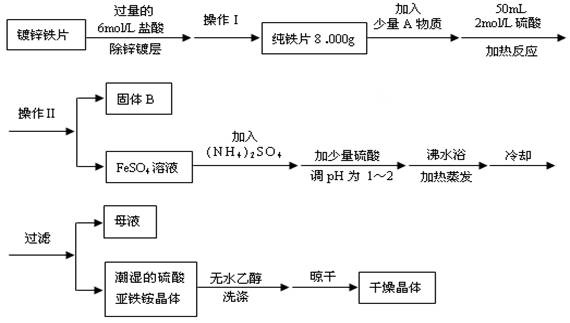
请回答下列问题:
(1)确定锌镀层被除去的标志是 ;
计算上述铁片锌镀层的厚度,不需要的数据是 (填编号)。
a.锌的密度ρ(g/cm3) b.镀锌铁片质量m 1(g) c.纯铁片质量m 2(g)
d.镀锌铁片面积S(cm2) e.镀锌铁片厚度h(cm)
(2)上述流程中:操作Ⅰ是取出铁片、 、 、称量。
(3)A物质可以为 (填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(4)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 。
(5)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入NaOH溶液,露置于空气中,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
答案
B
C
A
C
D
B
C
A
A
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确得2分,但只要选错一个就得0分)
题号
10
11
12
13
14
15
16
17
18
答案
BC
A
D
BD
AC
AC
C
C
BD
三、(本题包括3小题,共34分)
19.(一)(6分)
(1)热的Na2CO3会发生水解反应使溶液碱性,在碱性条件下使油脂充分水解而除去(2分)
(2) 浓缩至液体表面出现洁净薄膜(1分)
(3) 在相同温度下,(NH4)2SO4•FeSO4•6H2O的溶解度比(NH4)2SO4、FeSO4小(1分) ;
7(m1―m2)g (1分)
(二).(共5分)
(1)酸式(1分) 5Fe2+ + MnO4- + 8H+= 5Fe3++ Mn2+ + 4H2O(2分)
(2)当最后一滴KMnO4酸性溶液滴下时,溶液变成紫色,30s内不褪色,说明达到滴定终点(1分)
(3)1/V(1分)
20.(10分)
[交流与讨论](1)2AI+2NaOH+2H20=2NaAl02+3H2 ↑ (2分)
(2)97mL (2分)
(3)滤纸破损;过滤时漏斗里的液面高于滤纸边缘;仪器不干净等(1分)
(4)偏高 (1分)
[实验拓展](4分) 
21、(13分)
(1)①产生二氧化硫没有干燥,水蒸气会与Na2O2反应;②在B、C之间加一个装有NaOH溶液的洗气瓶 除去SO2气体(每空1分,共3分)
(2) 2Na2O2+2CO2=2Na2CO3+O2↑(2分)
①提出合理假设
假设1:白色固体为Na2SO3 假设2:白色固体为Na2SO3与Na2SO4 的混合物
假设3:白色固体为Na2SO4(每空1分,共3分)
② (每空1分,共5分)
实验操作
预期现象与结论
步骤1:取少量白色固体于试管,加入足量的稀盐酸
若闻到刺激性气味,说明白色固体含有Na2SO3.
步骤2:在步骤1的溶液加入足量的氯化钡溶液
若有白色沉淀生成,则说明白色固体含Na2SO4.
若步骤1现象明显,而步骤2没明显现象,则说明白色固体为Na2SO3;若步骤1现象不明显,步骤2现象明显,则说明白色固体为Na2SO4;若上述两个实验现象均有,则说明白色固体既含有Na2SO3,又含有Na2SO4。
四、(本题包括3小题,共34分)
22.(12分)
(1)硅(2分)(2)原子 ,C3N4 ,高温、高压 (各2分,共6分)
(3)4Al + 3O2 = 2Al2O3 IIA(各2分,共4分)
23(14分)
(1)CuO+2H+→Cu2++H2O(2分)
(2)烧杯、量筒(4分,各2分)
(3)SO2(2分)
(4)取少许样品,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有Cu2O,反之则没有(2分)
(5)铜粉的质量(2分) 最终所得CuO的质量(2分)。
24 (8分)
(1)NO2(g)+CO(g)=CO2(g)+NO(g) △H=-234kJ?mol-1(2分)
(2)①>(2分) ②C(2分)
(3)①N2H62++H2O [N2H5?H2O]++H+(2分)
[N2H5?H2O]++H+(2分)
五、(本题包括1小题,9分)
25(9分)
(1)C6H6(1分)
(2)碳碳双键 酯基 (每个1分,共2分)
(3)分别取少量粗品和纯品于试管,分别加入NaHCO3溶液,若试管中有气泡产生,则原试剂为粗品。(其它合理答案也给分)(2分)
 |
(4) (2分)
(5) ;
; (每个1分,共2分)
(每个1分,共2分)
六、选做题(本题包括2小题,每小题10分,考生只能选做一题)
26.(10分)
⑴加成反应 消去反应 取代反应 (3分)
⑵ +2NaOH→
+2NaOH→ +2NaBr (2分)
+2NaBr (2分)
⑶ ③; 保护A分子中C=C不被氧化
 (5分)
(5分)
27.(10分)
(1)1s22s22p63s23p6 (1分)
(2)ZCl<Ycl<XCl (1分)
(3) Cu 4 (每空2分,共4分)
(4) CH3―CH2―Cl中与Cl原子成键的C以sp3杂化,而CH2=CH2―Cl中与Cl原子成键的C以sp2杂化,电子云密度不同;CH3―CH2―Cl中的C―Cl的键长比CH2=CH2―Cl中C―Cl要长;CH2=CH2―Cl的∏键对Cl的作用力比CH3―CH2―Cl的a键强。
(答对两点给2分)
(5)HF沸点比HCl高;氢氟酸是弱酸,盐酸是强酸;实验测得HF分子质量偏大。
(答对两点给2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com