
题目列表(包括答案和解析)
(13分)为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。
(1)实验时,第一步实验操作为:将装有CaCO3干燥管下移与稀硝酸反应生成CO2,该操作作用为 。反应的化学方程式为 。
从装置的设计看,确定E中空气已被赶尽的实验现象是
。
(2)第二步,提起干燥管B, 将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明?
。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是 。
(4)装置D的作用是 。
(5)将一定量铜与足量稀硝酸充分反应,可以得到4.48L NO气体(气体体积在标准状况下测定),若反应后溶液体积为100mL,则所得溶液中Cu2+的物质的量浓度是
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,
其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。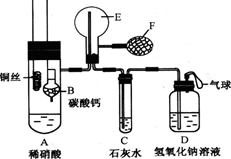
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: 。从装置的设计看,确定E中空气已被赶尽的实验现象是:______________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明? 。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是 。
(4)装置D的作用是 。
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。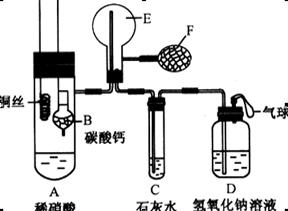
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: 。从装置的设计看,确定E中空气已被赶尽的实验现象是:______ ________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明?
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是
。
(4)装置D的作用是 。
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,
其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。

(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: 。从装置的设计看,确定E中空气已被赶尽的实验现象是:______________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明? 。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是 。
(4)装置D的作用是 。
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。
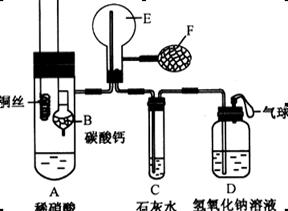
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: 。从装置的设计看,确定E中空气已被赶尽的实验现象是:______ ________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明?
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是
。
(4)装置D的作用是 。
1B
3D
5D
10BC
12AD
13BD
14BC
15.(12分)(1)x=1.5 (2)c(3)2Na2CO4=2Na2CO3+O2↑
(4)2CO42-+4H+=2CO2↑+O2↑+H2O
(5)g→h→e→f→d→c→b,
16.(8分)(1)CO(NH2)2 (2)AlO2-+CO2+H2O==Al(OH)3↓+HCO3-
(3)2Al2O3+2N2+
(4)CO2在水中的溶解度远小于NH3,若先通入CO2,则反应③中K的产率很低
17.(12分)(1)①(1分) (2)①②⑤(2分)
NO+NO2+2NaOH=2NaNO2+H2O(1分) 88.5%(2分)
(3)4FeS2+15O2+2H2O 2Fe2(SO4)3+2H2SO4(2分)
2Fe2(SO4)3+2H2SO4(2分)
Cu2S+10Fe3++4H2O 2Cu2++10Fe2++8H++SO42-(2分)
2Cu2++10Fe2++8H++SO42-(2分)
(4)3NO=N2O十NO2(1分),由于2NO2 N2O4,即生成的NO2又双聚成N2O4,导致气体分子数减少,使其压强路小于1.01×107 Pa的2/3(1分)
N2O4,即生成的NO2又双聚成N2O4,导致气体分子数减少,使其压强路小于1.01×107 Pa的2/3(1分)
18.(10分)(1)ABEF(2分)
(2)c(SO42-)>c(Fe2+)>c(H+)>c(OH-) (2分)
(3)硫酸作用Fe2+抑制的水解,铁皮的作用防止Fe3+的氧化。(2分,各1分)
(4)在试管中取滤液少许,加入足量的NaOH溶液,加热,用湿润的红色石蕊试纸检验,若试纸变兰色,则证明滤液中含有NH4+。(2分)
(5)FeSO4+2NH4HCO3 →FeCO3↓+( NH4)2 SO4+ CO2↑+H2O(2分)
19. (12分)(1)F: I:  (2分)(2)加成、消去 (2分)
(2分)(2)加成、消去 (2分)
 |
(4)4 (2分)
(5)
 |
20(8分)(1)Cu+2H++H2O2==Cu2++2H2O (2分) (2) 淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去。(2分)
(3)n(Cu)=1/2n(I2) = n(S2O32-)=6.45×0.01100=0.07095mmol
ωCu=0.07095×10-3×64×250.00/50.00/1.1=0.02064(4分)
21.(10分)(5)2分,其它每空1分
(1)Ar (2)极性 (3)5 1 (4)D是CH3OH,分子之间能形成氢键
(5)CO中第一个π键的键能是273kJ/mol,N2中第一个π键的键能是523.3kJ/mol,所以CO的第一个键比N2更容易断。
(6)1s22s22p63s23p6 3d104s1
(7)分子晶体
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com