
题目列表(包括答案和解析)
(1)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
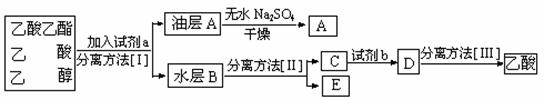
则试剂a是:____________,分离方法I是____________,分离方法II是____________,
试剂b是______________,分离方法III是____________。
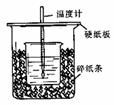
(2)用50mL0.50mol/L盐酸与50mL0.50mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
①.从实验装置上看,图中尚缺少的一种
玻璃用品 。
②.烧杯间填满碎纸条的作用是 。
③.如果用60mL0.50mol/L盐酸与60mL0.50mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”) 。
I.纯碱、烧碱等是重要的化工原料。
(1)利用上图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是___________________,
若其他操作不变,将A与C连接,可观察到的现象是__________________________。
(2)向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体的组成可能是:
A.NaOH和Na2CO3;B. ;C. ;D. 。
(3)设计实验确定(2)中白色固体中存在A项中的阴离子:
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| ② | | |

I.纯碱、烧碱等是重要的化工原料。

(1)利用上图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是___________________,
若其他操作不变,将A与C连接,可观察到的现象是__________________________。
(2)向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体的组成可能是:
A.NaOH和Na2CO3;B. ;C. ;D. 。
(3)设计实验确定(2)中白色固体中存在A项中的阴离子:
实验操作 | 实验现象 | 结论 |
①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 |
|
|
②
|
|
|
II.化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙,氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生。
牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应
后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气。其作用除了可搅拌B,C中的反应物外,还有: 。
(2)C中反应生成BaCO3的离子方程式是 。
(3)下列各项措施中,不能提高测定准确度的是( )
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A~B之间增添盛有浓硫酸的洗气装置
D.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为________。
(5)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是 _________________________________。
(6)装置中U形管D中的碱石灰的作用是_____________________________。
(14分)I 选择下列实验方法分离物质,将分离方法的序号依次为
①分离水和四氯化碳的混合物;②分离氯化钾溶液和沙子的混合物;
③从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
④ 分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)的混合物;
⑤分离食盐和碘的混合物; ⑥ 从碘水中提取碘单质。
A.过滤 B.结晶 C.分液 D.蒸馏 E.萃取分液 F.升华
II 、长期存放在Na2SO3会被空气中的氧气部分氧化。某化学兴趣小组通过实验测定某无水Na2SO3被氧化的程度。

请回答:(1)写出B装置中反应的离子方程式
(2)称量a g Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量BaC12溶液充分反应,过滤、洗涤、干燥、称量得白色沉淀b g,则样品中的Na2SO3的质量分数为 。
(3)深入研究发现,上述实验方案存在缺陷,致使测得的Na2SO3质量分数偏小,试分析其中的原因(列出一条即可) 。
(Ⅱ)乙同学设计了另一套实验装置如下图:

(4)实验中待锥形瓶中不再产生气体后,打开活塞P从导管左端缓缓鼓入一定量的空气,这样做的目的是 。
(5)除已称量的a g Na2SO3样品外,实验中还应测定的数据是 (填图中字母)装置实验前后的质量差。
(Ⅲ)现有以下试剂:蒸馏水、盐酸、稀硝酸、BaC12溶液、Ba(NO3)2溶液。
(6)丙同学欲从中选择合适试剂,来测定已知质量为a g的Na2SO3样品中Na2SO3的质量分数,下述实验方案理论上可行的有 。
A.将样品溶解,加足量盐酸,再加足量BaC12溶液,过滤、洗涤、干燥、称量沉淀m1g
B.将样品溶解,加足量盐酸,再加足量Ba(NO3)2溶液,过滤、洗涤、干燥、称量沉淀m2g
C.将样品溶解,加过量BaC12溶液,过滤后,将滤液蒸干,称量得固体m3g
D.将样品溶液,加过量Ba(NO3)2溶液,过滤、洗涤,在沉淀中加入足量盐酸,再过滤、洗涤、干燥、称量得固体m4g

| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | | |
| ② | | |

一、二选择题
1.B 2.C 3.D 4.C 5.B 6.A 7.D 8.C 9.C 10.B 11.D 12.C 13.D 14.BC 15AB
16C 17C 18C
19、(1)本实验要求无水操作,要求严密防止大气中的湿气进入本体系。
(2)不可行。如果塞紧,回流系统就成了封闭系统。封闭系统受热后,将会发生过热、冲料、爆炸、着火(酒精可燃)等意外事故。
(3)氯化钙可以用作吸水剂,但它受热后又可使结合的水再释出,达不到干燥的目的,又氯化钙也可以吸附乙醇。
(4)氧化钙跟水发生反应生成的氢氧化钙是不挥发的,受热也不分解,所以不影响蒸馏纯乙醇。
(5)冷凝管内管管壁等仪器的表面,,尚附有湿气,因此最初的几毫升蒸馏液可能含有的水份相对多一些,纯度达不到99.5%,所以另外收集,以免影响所收集乙醇的纯度
20、(1)碎瓷片,防止爆沸 (2)提高乙酸的转化率 (3)及时地蒸出生成物,有利于酯化反应向生成酯的方向进行 (4)a :饱和Na2CO3溶液;I :分液;II :蒸馏;b :硫酸;III :蒸馏 (5)①所加的NaOH溶液较少,没有将余酸中和 ②所加的NaOH溶液过量使酯完全水解。
21、CH3―CH=CH2;C6H5―CH2OH;HCOOH
22.(1).files/image039.jpg)
.files/image041.jpg)
.files/image043.jpg)
.files/image046.gif) 23.
23..files/image048.jpg)
(2)
(3)5
.files/image050.jpg)
24.⑴
.files/image052.jpg)
(或相应的间位、邻位)
⑵ .files/image054.jpg)
25.
.files/image056.gif) |
.files/image058.gif) 22.4
L?mol-1 = 76g?mol-1
22.4
L?mol-1 = 76g?mol-1由浓硫酸增重可知一定量A中氢原子的物质的量:.files/image060.gif)
由氧化铜减重可求知一氧化碳的物质的量:.files/image062.gif)
由石灰水增重可求知二氧化碳的量:.files/image064.gif)
一定量A中氧原子的物质的量为:
.files/image066.gif)
所以A的实验式为C2H4O3,其式量为76g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com