
题目列表(包括答案和解析)
“无土栽培”是一项利用化学试剂配成的营养液来栽培植物的新技术。下表是某实验小组的两种营养液的配方。请你回答有关问题:
| 配方Ⅰ | 配方Ⅱ |
| KCl 0.2g | KNO3 1.2g |
| KH2PO4 0.5g | Ca(NO3)2 1.4g |
| MgSO4 0.5g | (NH4)3PO4 0.3g |
| CaSO4 1.0g | MgSO4 0.6g |
| FeCl3 0.2g | |
| 备注:①各用2L水配制;②不用硬水配制 | |
(1)配方Ⅰ中属于复合肥料的物质是 ;
(2)判断所用的水是否是硬水的方法: ;
(3)从均衡养分的角度分析,选用 (填“配方Ⅰ”或“配方Ⅱ”)种植的同种植物在其他条件相同时长势会更好,其理由是 。
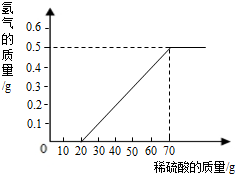 (2013?湛江)某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
(2013?湛江)某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com