
题目列表(包括答案和解析)
 我市濒临渤海,有较长的海岸线,海洋资源十分丰富.
我市濒临渤海,有较长的海岸线,海洋资源十分丰富.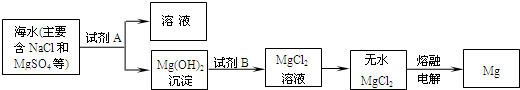
 我市濒临渤海,有较长的海岸线,海洋资源十分丰富.
我市濒临渤海,有较长的海岸线,海洋资源十分丰富.
我市濒临渤海,有较长的海岸线,海洋资源十分丰富。
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、 、 可制得精盐。
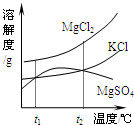
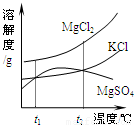
(2)晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线示意图。
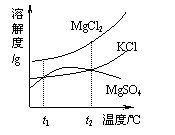
①设t1℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则它们的大小关系为 。
②将卤水加热到t2℃以上,根据溶解度曲线,首先析出的晶体是 。
(3)目前世界上60%的镁是从海水中提取的。其主要步骤如下:
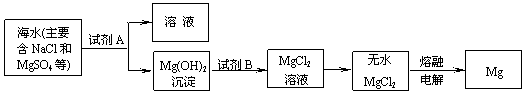 |
①提取Mg的过程中,试剂A可以选用_________,试剂B选用_________。
②分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去 ;加入过量Na2CO3溶液的目的是 。
(4)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是
。海底矿产资源“可燃冰”,其主要成分是水合甲烷晶体(CH4·nH2O),若水合甲烷晶体中CH4的质量分数为10%,则水合甲烷晶体的化学式为 。



一、选择题(本大题共10题,每小题2分,共20分)每小题给出的四个选项中,只有一个最符合题意,请将其序号涂在答题卡上。
题号
1
2
3
4
5
6
7
8
9
10
答案
B
B
C
D
C
C
B
D
A
D
二、选择题(本大题共5题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不给分;有2个选项符合题意的只选一个且符合题意给1分,若选2个有一个不符合题意则不给分。
题号
11
12
13
14
15
答案
B
B
B
BD
C
三、(本大题共5题 共29分)
16.(6分)(每空1分) (1)16 6 (2)2H Na+ (3)22 1:8
17.(7分)(每空1分) (1)天然气 (2)盖上锅盖 使可燃物与空气隔绝 (3)分别取少量样品至于试管中,加入少量食醋,若产生气泡的则是纯碱,无现象的是食盐。 (4)元素
(5)聚氯乙烯 (6)吸附
18.(5分)(每空1分) (1)①(2)①碳酸钙 水 ② ③能量
③能量
19.(9分)(每空1分,化学方程式2分) (1)分子之间有间隙(2)氧气 8:1
水是由氢、氧两种元素组成的。(其他合理答案也可给分) (3)蒸馏水
(4)煮沸水(5)过滤雨水中的固体杂质(6)
20.(2分) 89.9%
四、(本大题共4题 共31分)
21.(8分)每个化学方程式2分。
(1)Ca(OH)2 + CO2 ====CaCO3↓+ H2O
(4)2H2O2=====2H2O+O2↑
22.(9分)(每空1分) (1)①长颈漏斗 ②集气瓶 (2)AD或AE 固体与固体反应且需要加热;氧气的密度比空气略大,氧气不易溶于水(3)BE 将燃着的木条放在集气瓶口,若木条立即熄灭,证明二氧化碳已集满 A D (4)防止CO2溶于水(或防止CO2与水反应、防止CO2与水接触),没有
 23.(4分)(每空1分,化学方程式2分) (1)CuO (2)C+2CuO=====2Cu+CO2↑(3)不同
23.(4分)(每空1分,化学方程式2分) (1)CuO (2)C+2CuO=====2Cu+CO2↑(3)不同
24.(10分) (每空1分)
(1)过滤 蒸发 (2)①a>b=c ②MgSO4 (3)①氢氧化钠或氢氧化钙 盐酸 ②Na2SO4 除去CaCl2和过量的BaCl2(4)取样并滴加AgNO3溶液,若没有白色沉淀,说明蒸馏海水为淡水;CH4?8H2O
五、(本大题共2题 共10分)
25.(6分)解:设反应的锌的质量为x,生成的硫酸锌的质量为y。
Zn+H2SO4====ZnSO4+H2↑
65 161 2
x
y
65:x =2:
x =
y =
样品中铜的质量为
硫酸锌溶液的质量为
硫酸锌溶液的溶质质量分数为
答:略。
26.(4分)
(1)碳酸钙 ………1分
(2)产生的二氧化碳质量=
设盐酸中氯化氢的质量为x。
CaCO3+2HCl====CaCl2+H2O+CO2↑
73 44
x

x=
盐酸的溶质的质量分数=
答:略。
 |
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com