
题目列表(包括答案和解析)
| ① |
| ② |
| ③ |
 生石灰
生石灰 消石灰
消石灰 烧碱
烧碱| ① |
| ② |
| ③ |
 生石灰
生石灰 消石灰
消石灰 烧碱
烧碱某校化学小组对热水壶底部水垢的主要成分进行了'如下探究,请完成以下活动并回答相关问题。
【查阅资料】
天然水中含有![]() 、
、![]() 、
、![]() 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质――水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表:
部分钙、镁化合物溶解性表(20℃)
| 阴离子 阳离子 |
|
|
|
|
| 微溶 | 不溶 | 可溶 |
|
| 不溶 | 微溶 | 可溶 |
【提出猜想】
水垢的主要成分中一定含有 和 ,可能含有Ca(OH)2和MgCO3(填化学式)。
【设计方案】
实验1:确定水垢中是否含Ca(OH)2和CaCO3。
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液 | 没有白色沉淀产生 | _________________________ |
实验2:确定水垢是否含MgCO3。
利用下列实验装置,完成实验2探究。其主要实验步骤如下:
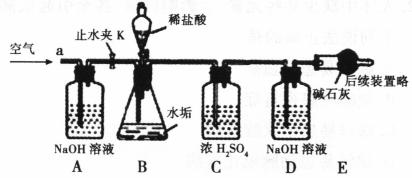
称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响)。
【实验讨论】
(1)加入样品前还应 ,装置B中盛放稀盐酸的仪器名称为 ,装置C的作用是 ,反应结束后打开止水夹K,缓缓鼓入空气的目的是 ,装置A的作用是 。A、B装置之间 设置干燥装置(填“要”、“不要”),其理由是 。
(2)装置B中生成气体的化学反应方程式为 (只要求写一种),装置D中的化学反应方程式为 。
(3)装置B中生成CO2的质量为 g。通过计算说明水垢中 含MgCO3(填字母)。
A.一定 B.一定不 C.可能 D.无法确定
计算过程(已知物质相对分子质量CaCO3:100,MgCO3:84):
实验3:确定水垢中是否含有Mg(OH)2。
另取质量为2.50g水垢,加3.65%稀盐酸与之反应,测得消耗稀盐酸![]() g。结合以上实验结论,判断当
g。结合以上实验结论,判断当![]() 的值满足 条件时,水垢中一定含有Mg(OH)2(请通过计算说明)。
的值满足 条件时,水垢中一定含有Mg(OH)2(请通过计算说明)。
一、选择题(本大题共10题,每小题2分,共20分)每小题给出的四个选项中,只有一个最符合题意,请将其序号涂在答题卡上。
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
D
A
D
D
C
D
B
C
二、选择题(本大题共5题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不给分;有2个选项符合题意的只选一个且符合题意给1分,若选2个有一个不符合题意则不给分。
题号
11
12
13
14
15
答案
D
C
AB
B
BC
三、(本大题共5题 共15分)
16.(5分)(每空1分) (1)① (2)③ (3)⑤ (4)② (5)④
17.(4分)(每空1分) 降低 吸水性 硝酸银溶液 稀硝酸
18.(1分)(每空1分) 碱
19.(2分)(每空1分) (1)碱性氧化物 碱 (2)酸性氧化物 酸 盐
20.(3分)(每空1分) Fe Cu Ag ;Fe2+ Zn2+ ;Ag+ Cu2+
四、(本大题共4题 共18分)
21.(8分)每个化学方程式1分,每空1分。化学方程式略。中和反应是(3)
22.(3分)每个化学方程式1分,化学方程式略。
23.(5分)(每空1分)(1)CuSO4 (2)Na2CO3 (3)BaSO4 (4)NaCl H2SO4和NaNO3 或H2SO4和Na2SO4
24.(2分)(每个正确答案1分)②③
五、(本大题共2题 共12分)
25.(6分)(每空1分) (1)化学方程式略 (2)C (3)铜 (4)CuSO4和H2SO4 (5)A
26.(6分)(每空1分) (1)二 (2)稀硝酸 确定溶液中是否存在碳酸根离子 硝酸钡 确定溶液中是否含有硫酸根离子 硝酸银
六、(本大题共3题 共15分)
27.(4分)(每空1分) 稀盐酸 稀盐酸 碳酸根离子 硫酸钡
28.(6分)(每空1分)
A Fe2O3 D Fe(OH)3 E
CO F CO
29.(5分)(每空1分)
A BaSO4 B
Ba(OH)
七、(本大题共2题 共10分)
30.(3分)解:设反应的硫酸铜质量为x
CuSO4+2NaOH====Cu(OH)2↓+Na2SO4
160 98
X

 X
X
X=
硫酸铜溶液的质量分数为
答:略。
31.(7分)
(1) 同意。 ………………1分
(2) Cu―Ag ………………1分
解:设合金中银的质量为X
Cu+2AgNO3====Cu(NO3)2+2Ag
64 216
64 216


X=
铜和银的质量比为(9.6-6.4)g :
(3)解:设参与反应的硝酸银的质量为X
Cu+2AgNO3====Cu(NO3)2+2Ag
64 340
64 340


Y=
硝酸银溶液的溶质质量分数为
答:略。
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com