
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
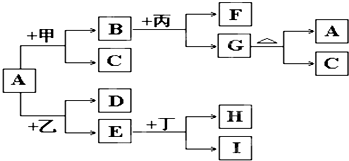
ШєДгH2SO4ЁЂNa2SO4ЁЂNa2CO3ЁЂNaClЁЂNaOHЁЂCu(NO3)2ЁЂHNO3 7жжШмвКжаШЁГіЦфжаЕФ2жжЃЌНјааЛьКЯМАгаЙиЪЕбщЃЌЫљЙлВьЕНЕФЯжЯѓвбМЧТМдкЯТБэжаЁЃЪдОнИїВНЪЕбщМАЦфЯжЯѓЯШНјааЗжВНЭЦЖЯ(МДЪЕбщНјааЕНИУВНЫљФмзїГіЕФФГЮяжЪПЯЖЈДцдкЁЂЗёЖЈДцдкЛђПЩФмДцдкЕФХаЖЯ)ЃЌдйзлКЯЭЦЖЯЫљШЁГіЕФ2жжШмвКЕФПЩФмзщКЯЁЃ
ВНжш | ЪЕбщВйзї | ЪЕбщЯжЯѓ | ЗжВНЭЦЖЯ |
ЂХ | НЋШЁГіЕФ2жжШмвКНјааЛьКЯ | ЛьКЯШмвКЮоЩЋЁЂГЮЧх ЮоЦфЫћУїЯдЯжЯѓ | ЛьКЯШмвКжаПЯЖЈВЛКЌCu(NO3)2 ЛьКЯШмвКПЯЖЈВЛЪЧЯТСазщКЯЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ |
ЂЦ | гУpHЪджНВтЖЈЛьКЯШмвКЕФpH | ВтЖЈНсЙћЃКpHЃН2 | |
ЂЧ | ЯђЛьКЯШмвКжаЕЮШызуСПBa(NO3)2ШмвК | гаАзЩЋГСЕэГіЯж | |
ЂШ | ЯђЩЯЪіШмвКЙ§ТЫЫљЕУЕФТЫвКжаЕЮМгAgNO3 | ЮоУїЯдЯжЯѓ |
ЛьКЯШмвКЕФПЩФмзщКЯЃЈаДГіШмжЪЕФЛЏбЇЪНЃЌгаМИзщаДМИзщЃЌВЛвЛЖЈЬюТњЃЌЃЉЃК
ЂйЁЁЁЁЁЁ КЭЁЁЁЁ ЁЁ ЃЛЂкЁЁЁЁ ЁЁ КЭ ЁЁЁЁЁЁЁЁ ЃЛЂлЁЁЁЁЁЁ КЭЁЁ ЁЁЁЁЁЁ ЃЛ
ЂмЁЁЁЁЁЁ КЭЁЁЁЁ ЁЁ ЃЛЂнЁЁЁЁ ЁЁ КЭ ЁЁЁЁЁЁЁЁ ЃЛЂоЁЁЁЁЁЁ КЭЁЁ ЁЁЁЁЁЁ ЃЛ
 ЗжБ№ЛиД№ЯТСаЮЪЬтЃЎ
ЗжБ№ЛиД№ЯТСаЮЪЬтЃЎ| O | 2- 4 |
| AЁЂЧтбѕЛЏФЦЙЬЬхгІЪЂЗХдкДјЯ№НКШћЕФЙуПкЪдМСЦПжа | BЁЂЪЕбщЪвЛюЦУН№ЪєKЁЂCaЁЂNaЦ№Л№ЃЌВЛФмгУЫЎУ№Л№ | CЁЂШєХЈH2SO4ВЛЩїНІШыблОІЃЌгІСЂМДгУХЈNaOHжаКЭВЂгУДѓСПЫЎГхЯД | DЁЂдВЕзЩеЦПВЛФмдкОЦОЋЕЦЩЯжБНгМгШШЃЌгІЕцЪЏУоЭј |
| ||
| ||
| 1 |
| 2 |
| ||
| ||
| ЗаЬкТЏЮТЖШ/Ёц | 600 | 620 | 640 | 660 |
| ПѓдќжаCuSO4ЕФжЪСПЗжЪ§/% | 9.3 | 9.2 | 9.0 | 8.4 |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com