
3.关于实验室制备乙烯的实验,下列说法中正确的是( )
A. 反应物是乙醇和过量的3mol/L硫酸的混合液
B. 温度计插入反应液液面下,控制温度为140℃
C. 反应容器(烧瓶)中应加入少量瓷片
D. 反应完毕先灭火再从水中取出导管
(考查学生对乙烯实验室制法的掌握和理解)
2. 在相同状况下,质量相同的乙烯和一氧化碳具有相同的( )
A.物质的量 B.原子个数
C.体积和密度 D.燃烧产物
(考查了气体摩尔质量与物理性质之间的关系)
1. 既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有乙烯的方法是( )
A.通入足量的溴水 B.与足量液溴反应
C.在导管口点燃 D.一定条件下与H2反应
(考查了甲烷和乙烯化学性质的区别)
2、(2000年上海高考)某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢原子直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。
已知: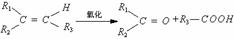
试写出:
⑴A的化学式
⑵化合物A和G的结构简式:A
B
⑶与G同类的同分异构体(含G)可能有 种。
(该题考查了学生对信息的转移能力和对烯烃结构的理解)3. 今有乙烷、丙烯、丁二烯的混合气体若干摩,充分燃烧后,耗O2为相同状况下混合气体体积的5倍。 (1)求混合气体符合要求的可能配比。(配比写成最小整数比,且每个整数大于0,小于8)_____ 、 、 _________(写三种) (2)若混合气中乙烷、丙烯、丁二烯的物质的量分别为n1,n2,n3,则三者必须满足的函数关系是______________(用带有n1,n2,n3的等式表示)
(该题考查了烃的燃烧通式的计算,解题时从烃的燃烧通式入手,充分利用题目中所给的条件不难得到正确结论)
新活题网站
3、乙烯、乙炔的实验室制取:
掌握反应原理、发生装置 、收集方法及实验过程中的注意事项。 4、烯烃、炔烃的性质: 物理性质一般随分子里碳原子数的增多而呈规律性变化,如沸点随碳原子数的增加而升高,液态时的密度随随碳原子数的增加而增大。化学性质分别与乙烯和乙炔相似。 典型例题点击: 1. 已知碳原子数小于或等于8的单烯烃与HBr反应,其加成产物只有一结构。
①符合此条件的单烯烃有 种,判断的依据是
②在这些单烯烃中,若与H2加成后,所得烷烃的一卤代物的同分异构体有3种。这样的单烯烃的结构简式
(考查了单烯烃的结构的对称性。 解题时以“C=C”为中心向外延伸从而得出正确答案)
2.乙烯和乙炔的化学性质:
(1)氧化反应:
①燃烧反应
C2H4+3O2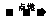 2CO2+2H2O
2CO2+2H2O
2C2H2+5O2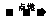 4CO2+2H2O(温度高达3000℃以上)
4CO2+2H2O(温度高达3000℃以上)
②常温易被氧化剂氧化。(使酸性高锰酸钾溶液褪色)
(2)加成反应:
①乙烯的加成反应:
CH2=CH2+Br2 CH2Br-CH2Br(常温下使Br2水褪色)
CH2Br-CH2Br(常温下使Br2水褪色)
CH2=CH2+HCl CH3-CH2Cl(制氯乙烷)
CH3-CH2Cl(制氯乙烷)
CH2=CH2+H-OH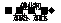 CH3CH2OH(制酒精)
CH3CH2OH(制酒精)
②乙炔的加成反应:
CH≡CH+Br2 CHBr=CHBr
CHBr=CHBr
CHBr=CHBr+Br2 CHBr2-CHBr2(常温下使Br2水褪色)
CHBr2-CHBr2(常温下使Br2水褪色)
CH≡CH+2H2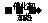 CH3-CH3
CH3-CH3
CH≡CH+HCl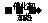 CH2=CHCl(制聚氯乙烯的单体)
CH2=CHCl(制聚氯乙烯的单体)
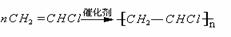
(3)聚合反应:
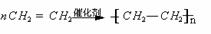
1.乙烯、乙炔的分子结构:(填表)
|
|
乙烯 |
乙炔 |
|
电子式 |
|
|
|
结构式 |
|
|
|
结构简式 |
|
|
|
分子构型 |
|
|
15.(1)133.9
(2)3m3<V<4m3
(3)设H2O为Xmol,O2为Ymol
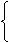
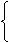 则 X+2Y=25
X=10
则 X+2Y=25
X=10
3X+4Y=60 Y=7.5
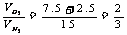
(4)设富氧空气中O2的体积分数为a,反应中用去H2O(g)与富氧空气的体积分别为X、Y。

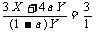

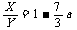
14.(1)3,4,6-三甲基-5-乙基辛烷;
(2)3,3-二甲基-5,5-二乙基辛烷
(3)2,2,4-三甲基-3-乙基庚烷
11.从题意可知,只要烃分子中氢原子数相同即可。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com