
有40克盐酸和![]() 的混合液,向其中滴加质量分数为20%的
的混合液,向其中滴加质量分数为20%的![]() 溶液,所加
溶液,所加![]() 溶液的质量与生成沉淀的质量关系如下图所示。
溶液的质量与生成沉淀的质量关系如下图所示。
求:(1)原溶液中![]() 的质量。
的质量。
(2)求生成沉淀的最大质量。

科目:初中化学 来源: 题型:解答题
 六一儿童节快到了,小芳打算帮妈妈做些家务,她想把厨房中盛有淀粉、食盐、纯碱、小苏打的调料盒贴上标签.请你帮助小芳完成如下探究过程:
六一儿童节快到了,小芳打算帮妈妈做些家务,她想把厨房中盛有淀粉、食盐、纯碱、小苏打的调料盒贴上标签.请你帮助小芳完成如下探究过程:| 实验现象 样品 所加试剂 | A | C | D |
| ______ | 无现象 | 有气泡 | ______ |

温度 盐 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |

| 实验操作 | 实验现象 | 结论 |

查看答案和解析>>
科目:初中化学 来源: 题型:
酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不 同温度下氢氧化钠的溶解度:
同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 。20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不 饱和”),其溶液的质量是 克。
饱和”),其溶液的质量是 克。
(2)在学习过程中,可以判断反应发 生的方法有多种。
生的方法有多种。
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
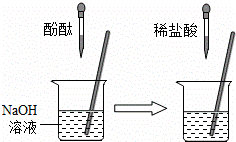
②在右图的实验中,当观察到的现象是
就可证明NaOH与HCl发生了反应。
③不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不 同温度下氢氧化钠的溶解度:
同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 。20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不 饱和”),其溶液的质量是 克。
饱和”),其溶液的质量是 克。
(2)在学习过程中,可以判断反应发 生的方法有多种。
生的方法有多种。
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
②在右图的实验中,当观察到的现象是
就可证明NaOH与HCl发生了反应。
③不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 .20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不饱和”),其溶液的质量是 克.
(2)在学习过程中,可以判断反应发生的方法有多种.
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应.
②在如图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应.
③不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com