
 随着人们生活水平的不断提高,汽车已走进千家万户.制造汽车要用到含铜、铁、铝等成分的多种金属材料.
随着人们生活水平的不断提高,汽车已走进千家万户.制造汽车要用到含铜、铁、铝等成分的多种金属材料.
| ||
| 10g-2g |
| 10g |
| 160 |
| 8g |
| 325 |
| x |
| 16.25g |
| 8g+109.5g |
| ||
| 10g-2g |
| 10g |
| 160 |
| 8g |
| 325 |
| x |
| 16.25g |
| 8g+109.5g |


科目:初中化学 来源: 题型:
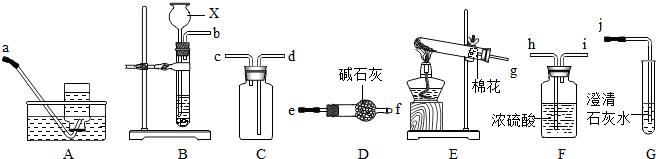
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物质 编号 | 甲 | 乙 | 丙 | 丁 | 物质转化关系 |
| A | CaCO3 | CaO | Ca(OH)2 | CaCl2 | 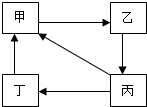 |
| B | CuSO4 | CuCl2 | Cu(OH)2 | CuO | |
| C | Fe | FeCl2 | Fe(OH)2 | Fe2O3 | |
| D | Zn | ZnO | ZnCl2 | Zn(NO3)2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、Ba(OH)2 |
| B、FeCl3 |
| C、HCl |
| D、Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
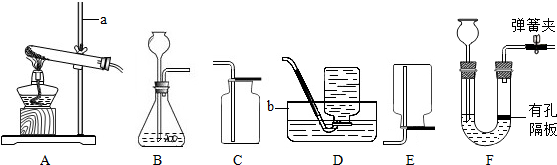
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com