
| A. | 15.3% | B. | 32.4% | C. | 49.3% | D. | 52.6% |
分析 根据铁与硫酸铜反应的方程式以及铁的质量,列比例式即可求得反应生成的铜以及硫酸亚铁的质量;根据质量守恒定律求得反应后溶液的质量,利用$\frac{溶质质量}{溶液质量}$×100%即可求得反应后所得溶液的溶质质量分数
解答 解:设生成铜的质量为x,生成FeSO4的质量为y.
Fe+CuSO4═FeSO4+Cu
56 152 64
5.6g y x
$\frac{56}{5.6g}=\frac{152}{y}=\frac{64}{x}$
解得:x=6.4g,y=15.2g
根据质量守恒定律,反应后所得溶液的质量为:100g+5.6g-6.4g=99.2g,
则反应后所得溶液的溶质质量分数为:$\frac{15.2g}{99.2g}$×100%=15.3%.
答:反应后所得溶液的溶质质量分数为15.3%.
故选:A.
点评 本题考查了质量分数的计算以及根据化学方程式的简单计算,写好化学方程式是解题的关键.注意化学变化都遵循质量守恒定律,质量守恒定律的灵活使用,对于解答此类问题会有很大帮助,甚至起到决定性作用.


科目:初中化学 来源: 题型:解答题
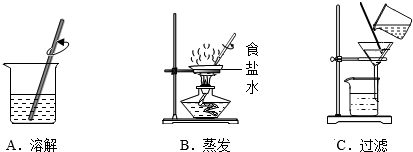
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用火碱溶液吸收二氧化硫SO2+2NaOH═Na2SO3+H2O | |
| B. | 植物的光合作用C6H12O6+6O2 $→_{光照}^{叶绿素}$6CO2+6H2O | |
| C. | 碳酸饮料中碳酸的形成原理CO2+H2O═H2CO3 | |
| D. | 利用一氧化碳的还原性得到金属铁2Fe2O3+3CO═4Fe+3CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
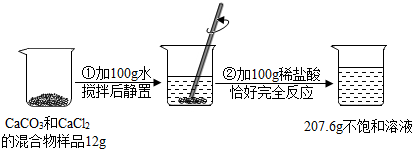
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示a~g是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知a是人体胃液中含有的酸,g是最轻的气体,b、c、d、e、f都是氧化物.其中e和f反应的生成物常用于改良酸性土壤,c和d发生的反应是工业上冶炼铁的主要反应原理之一.
如图所示a~g是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知a是人体胃液中含有的酸,g是最轻的气体,b、c、d、e、f都是氧化物.其中e和f反应的生成物常用于改良酸性土壤,c和d发生的反应是工业上冶炼铁的主要反应原理之一.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com