【答案】
分析:检查B装置的气密性的方法是:从长颈漏斗内加水形成液封,先把导管的一端插入水中,然后两手紧握试管的外壁,如果导管口有气泡冒出,证明装置严密;制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO
2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.在常温下,用硫化亚铁固体和稀硫酸制取硫化氢气体,因此不需加热;硫化氢是密度比空气大的有毒气体,溶于水,所以应用F装置收集;细木棒能够向上冲出的原因是:液体药品遇到黑色固体生成气体,瓶内压强增大,因此细木棒能够向上冲出;装置中可能是过氧化氢和二氧化锰,在二氧化锰做催化剂的条件下反应生成水和氧气,配平即可.白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是先下降后液面上升,因为燃烧时温度高,气体体积膨胀,因此液面下降;当冷却后,液面上升;若实验非常成功,最终集气瓶中水的体积约为70mL;集气瓶里预先装进的50mL水,在实验过程中起到的作用是:加快集气瓶冷却;液封导气管末端以防气体逸出;缓冲集气瓶内气压的骤然升高.
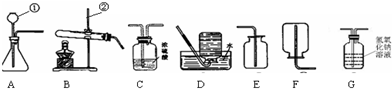
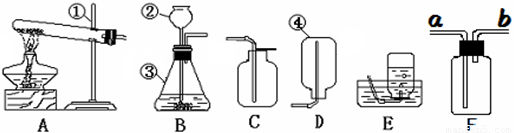
解答:解:(1)铁架台是夹持仪器,长颈漏斗方便加液体药品,锥形瓶是常用的反应容器,集气瓶是收集气体的仪器,故答案为:铁架台;长颈漏斗;锥形瓶;集气瓶
(2)制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:2KClO
3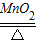
2KCl+3O
2↑;C或E
(3)检查B装置的气密性的方法是:从长颈漏斗内加水形成液封,先把导管的一端插入水中,然后两手紧握试管的外壁,如果导管口有气泡冒出,证明装置严密;故答案为:从长颈漏斗内加水形成液封,先把导管的一端插入水中,然后两手紧握试管的外壁,如果导管口有气泡冒出,证明装置严密;
(4)在常温下,用硫化亚铁固体和稀硫酸制取硫化氢气体,因此不需加热;硫化氢是密度比空气大的有毒气体,溶于水,所以应用F装置收集;故答案为:B;F
(5)细木棒能够向上冲出的原因是:液体药品遇到黑色固体生成气体,瓶内压强增大,因此细木棒能够向上冲出;装置中可能是过氧化氢和二氧化锰,在二氧化锰做催化剂的条件下反应生成水和氧气,配平即可;故答案为:液体药品遇到黑色固体生成气体,瓶内压强增大,因此细木棒能够向上冲出;2H
2O
2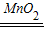
2H
2O+O
2↑;
(6)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是先下降后液面上升,因为燃烧时温度高,气体体积膨胀,因此液面下降;当冷却后,液面上升;若实验非常成功,最终集气瓶中水的体积约为70mL;集气瓶里预先装进的50mL水,在实验过程中起到的作用是:加快集气瓶冷却;液封导气管末端以防气体逸出;缓冲集气瓶内气压的骤然升高;故答案为:①先下降后液面上升;70;②abc
点评:本考点主要考查了检查装置的气密性、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和空气中氧气成分的测定等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

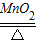 2KCl+3O2↑;C或E
2KCl+3O2↑;C或E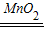 2H2O+O2↑;
2H2O+O2↑;

 步步高达标卷系列答案
步步高达标卷系列答案