
��6�֣���ѧ��ȤС��ͬѧ����ʵ��̨�ϰ�����˳��ڷ���7ƿ��ͬ����ɫ��Һ����ͼ��ʾ��������4��5���Լ�ƿ��ǩ����

��������⡿����ƿ�Լ��ijɷֱַ���ʲô��
���������ϡ��ټ��Ե��������ƣ�Na2SO3����Һ��Na2CO3��Һ�����Ե�CaCl2��Һ���ɷ������ֽⷴӦ��������ɫ������
��Na2SO3 + 2HCl="2NaCl" + SO2�� + H2O��
��CO2��SO2������ʹ����ʯ��ˮ����ǡ�
���������롿���������ǩ����Ϣ���Ʋ�4��5����Һ���ֱܷ���NaOH��Һ��Na2CO3��Һ��Na2SO3��Һ��NaCl��Һ�е�һ�֡�
��ʵʩ��������ȡ����4��5����Һ���Թ��У��ֱ������������ʵ�顣

������ʵ�顿Ϊ�˽�һ��ȷ��4��5����Һ�ijɷ֣�ͬѧ�Ƿֱ�ȡ����4��5����Һ���Թ��м���ʵ�顣

��ʵ�鷴˼��ͬѧ�Ǿ���������Ϊ4����Һ�������DZ��ʵ�NaOH��Һ���������������ʵ�鷽��������֤�����������ʵ�鱨�档
|
ʵ����� |
ʵ������ |
ʵ����� |
|
|
|
4����Һ�Dz��ֱ��ʵ�NaOH��Һ�� |
��ʵʩ������ ʵ��1 1 NaCl
ʵ��2 Na2CO3 + Ca(OH)2 = CaCO3��+ 2NaOH
����Na2SO3 + Ca(OH)2 = CaSO3��+ 2NaOH��
������ʵ�顿�������ݲ�����5����Һ�����д̼�����ζ�����塣
��ʵ�鷴˼����2�֣�ÿ���������������ȫ�߸�1�֣�
|
ʵ����� |
ʵ������ |
ʵ����� |
|
��ȡ����4����Һ���Թ��У���������CaCl2��Һ�� �����ϲ���Һ�еμ���ɫ��̪��Һ�� |
���а�ɫ�������� ����Һ����ɫ��ɺ�ɫ |
4����Һ�Dz��ֱ��� ��NaOH��Һ�� |
��������
���������ʵ��1����ȡ����4��5����Һ���Թ��У��ֱ�μӷ�̪��Һ����Һ�����ɫ��˵��4��5�Ų��������Ȼ�����Һ��
ʵ��2����ȡ����4��5����Һ���Թ��У��ֱ�μ�ʯ��ˮ�����а�ɫ����������4��5����Һ�������������ƻ���̼������Һ������һ����Ӧ�Ļ�ѧ����ʽΪNa2CO3 + Ca(OH)2 = CaCO3��+ 2NaOH������Na2SO3 + Ca(OH)2 = CaSO3��+ 2NaOH��
������ʵ�顿��ȡ����4��5����Һ���Թ��У��ֱ�μ�ϡ���ᣬ�������ݲ�����5����Һ�����д̼�����ζ�����壬4����̼������Һ��5��������������Һ��
��ʵ�鷴˼��Ϊ����֤4����Һ�Ƿ��Dz��ֱ��ʵ�����������Һ�������ձ���ʵ����֤��
|
ʵ����� |
ʵ������ |
ʵ����� |
|
��ȡ����4����Һ���Թ��У���������CaCl2��Һ�� �����ϲ���Һ�еμ���ɫ��̪��Һ�� |
���а�ɫ�������� ����Һ����ɫ��ɺ�ɫ |
4����Һ�Dz��ֱ��� ��NaOH��Һ�� |
���㣺����̽����ʵ�������̽�������ָʾ�����������ơ�̼���ơ��������Ƶ����ʡ�
��������̪�����ָʾ���������������ʻ��������ʲ���ɫ�������������ʱ��ɫ��


 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2009?�³�����ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ���У�����CO2������������ͼ��ʾ��
��2009?�³�����ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ���У�����CO2������������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
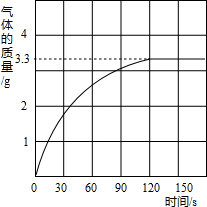 ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ���У�����CO2����������ͼ��ʾ��
ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ���У�����CO2����������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
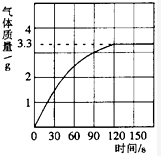 ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽10gˮ���У�����CO2����������ͼ��ʾ��
ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽10gˮ���У�����CO2����������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?������һģ��ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽10gˮ���У�����CO2����������ͼ��ʾ��
��2012?������һģ��ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽10gˮ���У�����CO2����������ͼ��ʾ�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ������CO2����������ͼ��ʾ��
ijУ��ѧ��ȤС��ͬѧ���֣�����ʹ�õ���ˮ���ײ���һ��ˮ����ˮ������Ҫ�ɷ���̼��ƺ�������þ������Ϊ�˲ⶨˮ����̼��Ƶĺ�������������������Ϊ10%��������뵽12.5gˮ������CO2����������ͼ��ʾ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com