
 Fe3O4;
Fe3O4; ;
;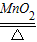 2KCl+3O2↑;
2KCl+3O2↑; Fe3O4;(1)氮气;红磷的量不足,装置漏气;(3)用凹透镜将太阳光聚焦引燃红磷,避免因拨出橡皮塞引燃红磷造成气体逸出,造成实验误差,同时还可避免五氧化二磷逸散到空气中污染空气,节省能源,无污染;(1)试管,酒精灯,2KClO3
Fe3O4;(1)氮气;红磷的量不足,装置漏气;(3)用凹透镜将太阳光聚焦引燃红磷,避免因拨出橡皮塞引燃红磷造成气体逸出,造成实验误差,同时还可避免五氧化二磷逸散到空气中污染空气,节省能源,无污染;(1)试管,酒精灯,2KClO3 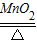 2KCl+3O2↑;(2)A,将带火星的木条放在集气瓶口,若带火星的木条复燃,说明收集已满;(3)Zn+H2SO4═ZnSO4+H2↑,C,E.
2KCl+3O2↑;(2)A,将带火星的木条放在集气瓶口,若带火星的木条复燃,说明收集已满;(3)Zn+H2SO4═ZnSO4+H2↑,C,E.

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 在“氧气的制取和性质”实验课中,某同学取一段纱窗网上的细铁丝,在自已收集到的氧气中做铁丝在氧气中燃烧的实验.?
在“氧气的制取和性质”实验课中,某同学取一段纱窗网上的细铁丝,在自已收集到的氧气中做铁丝在氧气中燃烧的实验.?查看答案和解析>>
科目:初中化学 来源: 题型:
 已知铁丝在氧气中可以发生反应:铁+氧气
已知铁丝在氧气中可以发生反应:铁+氧气| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 点燃 |
| 点燃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com