
实验室利用
98%的浓硫酸配制20%的硫酸溶液100g,一定不需要的仪器是[
]|
A .20mL量筒 |
B .100mL量筒 |
|
C .托盘天平 |
D .烧杯 |
科目:初中化学 来源: 题型:



查看答案和解析>>
科目:初中化学 来源: 题型:

| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: 使氧化铜完全反应 |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是: CuSO4、H2SO4 |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?金华)某同学为比较镁和铝的金属活动性强弱,将两块表面积相同并除去氧化膜的镁条、铝条分别与相同体积、相同质量分数的稀硫酸反应,测定两种金属与稀硫酸反应得到相同体积氢气所需要的时间.
(2013?金华)某同学为比较镁和铝的金属活动性强弱,将两块表面积相同并除去氧化膜的镁条、铝条分别与相同体积、相同质量分数的稀硫酸反应,测定两种金属与稀硫酸反应得到相同体积氢气所需要的时间.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
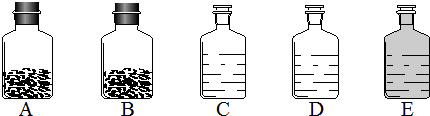
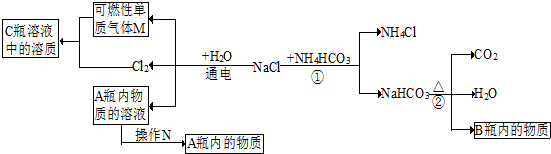
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com