
潍坊有丰富的海洋资源,氯化钠占整个海洋盐类的80%以上。下列有关氯化钠的说法正确的是( )
A. 室温下的氯化钠饱和溶液不能再溶解氯化钾
B. 取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和
C. 可用水鉴别氯化钠和氢氧化钠
D. 将100 g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器只有烧杯、量筒、玻璃棒
C 【解析】 A、一定温度下,一种物质的饱和溶液还能继续溶解其它物质,室温下的氯化钠饱和溶液还能再溶解氯化钾,故选项说法错误;B、溶液具有均一性,取出部分上层溶液,接近饱和的氯化钠溶液仍为不饱和溶液,故选项说法错误;C、氯化钠溶于水温度几乎不变,氢氧化钠溶于水温度升高,可以用水鉴别,故选项说法正确;D、利用浓溶液配制稀溶液,采用的加水稀释的方法,其操作步骤是计算、量取、溶解,所用的仪器...科目:初中化学 来源:湖北省武汉市七校联考2018届九年级上学期期中化学试卷 题型:计算题
地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,请回答:
(1)每个黄曲霉素B2的分子中含有_____个原子,黄曲霉素B2相对分子质量为_____;
(2)黄曲霉素B2中碳、氢、氧三种元素的质量比为_____;
(3)黄曲霉素B2中氧元素的质量分数是_____;
(4)15.7g黄曲霉素B2中含有_____g碳元素。
37314102:7:4830.6%10.2g 【解析】 (1)每个黄曲霉素B2分子是由17个碳原子、14个氢原子和6个氧原子构成的,则每个黄曲霉素B2的分子中含有37个原子;黄曲霉素B2的相对分子质量为12×17+1×14+16×6=314;(2)黄曲霉素B2中碳、氢、氧三种元素的质量比为(12×17):(1×14):(16×6)=102:7:48;(3)黄曲霉素B2中氧元素的质量分...查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学4.2化学反应中的质量变化同步测试卷 题型:填空题
煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露.乙硫醇在煤气燃烧过程中也可充分燃烧,其反应方程式为2C2H5SH+9O2  4CO2+2X+6H2O,则 X 的化学式为:________.
4CO2+2X+6H2O,则 X 的化学式为:________.
查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学:第九单元测试卷 题型:科学探究题
仔细阅读下面的探究实验信息,回答相关问题。
Ⅰ.(实验目的)探究溶解过程中,溶液温度的变化情况。
Ⅱ.(查阅资料)
(1)物质溶解于水的过程包括吸收热量(Q吸)的扩散过程和放出热量(Q放)的水合过程。
(2)实验条件下,水的凝固点为0 ℃、沸点为100 ℃。
Ⅲ.(提出猜想)物质溶解过程中,溶液的温度可能升高或降低或不变。
Ⅳ.(实验探究)某探究小组的同学设计了如下图所示的两种实验方案。在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在_____ ℃。
Ⅴ.(实验结论)图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度_____ (填“升高”“降低”或“不变”,下同)。图2所示实验中,若加入物质b后,热水会突然沸腾,说明_____。

Ⅵ.(拓展实验)按照图3所示进行实验。若物质c为NaOH,则U形管内的左边液面将_____ (填“高于”“低于”或“等于”)右边液面;若U形管内的液面位置变化与之相反,则物质c为_____ (填序号)。
①CaO ②NH4NO3 ③浓H2SO4
99降低溶液的温度升高低于② 【解析】 Ⅳ.【实验探究】由图中的条件可知:在图2所示方案中,每次加入物质b之前,均使用温度计控制热水温度,使之保持在99℃; Ⅴ.图1所示实验中,若加入物质a后,发现玻璃片与烧杯底部之间的水结冰,说明溶液的温度下降; 图2所示实验中,若加入物质b后,热水会突然沸腾,说明溶液的温度升高; Ⅵ.若物质c为NaOH,氢氧化钠溶于水放热,装置内...查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学:第九单元测试卷 题型:填空题
用“饱和”和“不饱和”填空。
(1)把硝酸钾晶体放到硝酸钾溶液里,晶体减少,则原硝酸钾溶液为_________溶液。
(2)将常温下配制的硝酸钾饱和溶液升温到80 ℃,则变成_________溶液。
(3)在10 ℃时,硝酸钾溶液中含有少量硝酸钾晶体,则该溶液为硝酸钾的_________溶液。
(4)将50 ℃时接近饱和的硝酸钾溶液降温到10 ℃,则溶液变为硝酸钾的_________溶液。
(5)在20 ℃时硝酸钾的饱和溶液中加入5 g水,则溶液变为硝酸钾的_________溶液。
不饱和不饱和饱和饱和不饱和 【解析】 (1)把硝酸钾晶体放到硝酸钾溶液里,晶体减少,说明原溶液还能继续溶解硝酸钾,则原硝酸钾溶液为不饱和溶液; (2)硝酸钾的溶解度随温度的升高而增大,所以将常温下配制的硝酸钾饱和溶液升温至80℃,则变为不饱和溶液; (3)在10℃时的硝酸钾溶液中含有少量硝酸钾晶体,则该溶液为硝酸钾的饱和溶液; (4)硝酸钾的溶解度随温度的降低而减小,...查看答案和解析>>
科目:初中化学 来源:广东省2019届九年级化学:第九单元测试卷 题型:单选题
用浓盐酸配制一定溶质质量分数的稀盐酸,实验时必不可少的一组仪器是( )
A. 玻璃棒 量筒 烧杯 胶头滴管 B. 托盘天平 量筒 烧杯 玻璃棒
C. 托盘天平 玻璃棒 烧杯 胶头滴管 D. 量筒 烧杯 漏斗 玻璃棒
A 【解析】 试题A、配制定溶质质量分数的稀盐酸,用到的仪器有:玻璃棒 量筒 烧杯 胶头滴管,正确;B、不用托盘天平称量固体药品,错误;C、不用托盘天平称量固体药品,错误;D、不用漏斗,错误。故选A查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学第七章应用广泛的酸、碱、盐 单元测试卷 题型:综合题
利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数. 下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
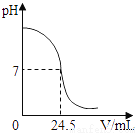
(1)根据下图曲线可以判断实验中是向________(填“酸”或“碱”,下同)溶液(待测液)中滴加________溶液(标准液).
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到________,则证明中和反应正好完成.
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数.
碱;酸碱溶液的红色刚好褪去3.6%. 【解析】 由图中溶液的pH变化情况,未加入时溶液的pH大于7,显碱性,后来溶液的pH逐渐减小,最终小于7,故开始是碱性溶液,过程中向碱溶液中滴加酸溶液,故填:碱,酸。 酚酞遇碱性溶液会变红,遇中性溶液不变色,中和反应刚好完成时溶液显中性,此时红色褪为无色,故填:碱溶液的红色刚好褪去。 设待测液溶质的质量分数为x, 2NaOH+H2...查看答案和解析>>
科目:初中化学 来源:沪教版九年级上册化学第七章应用广泛的酸、碱、盐 单元测试卷 题型:单选题
钾肥能促进作物茎秆粗壮,增强对病虫害和倒伏的抵抗能力。下列物质中能用作钾肥的是( )
A. 尿素〔CO(NH2)2〕 B. 硝酸铵(NH4NO3)
C. 磷酸二氢钙〔Ca(H2PO4)2〕 D. 硫酸钾〔K2SO4〕
D 【解析】 考点定位本题的考点是常见化肥的种类和作用。含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。 解答过程判断属于哪种化学肥料,关键要看化肥中含N、P、K元素中的哪一种。若含N,则是氮肥;若含P,则是磷肥;若含K,则是钾肥;若含N、P、K元素中的两种或两种以上,则是复合肥。结合题意...查看答案和解析>>
科目:初中化学 来源:2019届九年级沪教版化学全册第三章单元测试卷 题型:简答题
请结合下表回答下列问题。

(1)碳原子、氮原子、氧原子的质子数分别为________、________、________。
(2)五氧化二磷中磷元素的化合价为________。
(3)与磷元素化学性质相似的是____________元素。
678+5氮 【解析】 (1)原子的质子数等于原子序数,故碳原子、氮原子、氧原子的质子数分别为6、7、8。 (2)五氧化二磷中氧元素的化合价为+2价,设磷元素的化合价为x,根据化合价的代数和为0得,2×x+(-2)×5=0,x =+5. (3)磷元素的最外层的电子数是5,元素的化学性质与最外层的电子数有关,氮元素的最外层的电子数也是5,故与磷元素化学性质相似的是氮元素。 ...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com