水的硬度表示方法是:将水中的Ca2+、Mg2+质量折算成CaO的质量.通常把1L水中含有10mg CaO称为1度,1L水中含有20mg CaO即为2度,以此类推.8度以上为硬水,8度以下为软水.我国规定饮用水的硬度不能超过25度.
(1)日常生活中,可用______检验某水样是硬水还是软水.
(2)Ca(HCO3)2加热时会分解产生一种白色沉淀(水垢的主要成分)和两种常见的氧化物,请写出发生反应的化学方程式______ CaCO3↓+H2O+CO2↑
【答案】
分析:(1)根据硬水与软水的检验方法进行分析解答即可.
(2)由题意,Ca(HCO
3)
2加热时会分解产生一种白色沉淀(水垢的主要成分)和两种常见的氧化物,水垢的主要成分是碳酸钙;由质量守恒定律,两种常见的氧化物应为水和二氧化碳,写出反应的化学方程式即可.
(3)水垢的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,写出反应的化学方程式即可.
(4)石灰石的主要成分在雨水和二氧化碳的共同作用下生成了可溶的Ca(HCO
3)
2,写出反应的化学方程式即可.
解答:解:(1)生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水.
(2)由题意,Ca(HCO
3)
2加热时会分解产生一种白色沉淀(水垢的主要成分)和两种常见的氧化物,水垢的主要成分是碳酸钙;由质量守恒定律,两种常见的氧化物应为水和二氧化碳,反应的化学方程式2Ca(HCO
3)
2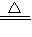
CaCO
3↓+H
2O+CO
2↑;河水、井水中溶有一定量的Ca(HCO
3)
2,可采取加热煮沸的方法使钙离子沉降来降低水的硬度.
(3)水垢的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑.
(4)石灰石的主要成分在雨水和二氧化碳的共同作用下生成了可溶的Ca(HCO
3)
2,反应的化学方程式为:CaCO
3+H
2O+CO
2═Ca(HCO
3)
2.
故答案为:(1)肥皂水;(2)2Ca(HCO
3)
2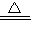
CaCO
3↓+H
2O+CO
2↑;加热煮沸;(3)CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑;(4)CaCO
3+H
2O+CO
2═Ca(HCO
3)
2.
点评:本题难度不大,了解硬水与软水的检验方法、化学方程式的书写方法是正确解答本题的关键.

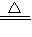 CaCO3↓+H2O+CO2↑;河水、井水中溶有一定量的Ca(HCO3)2,可采取加热煮沸的方法使钙离子沉降来降低水的硬度.
CaCO3↓+H2O+CO2↑;河水、井水中溶有一定量的Ca(HCO3)2,可采取加热煮沸的方法使钙离子沉降来降低水的硬度.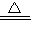 CaCO3↓+H2O+CO2↑;加热煮沸;(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)CaCO3+H2O+CO2═Ca(HCO3)2.
CaCO3↓+H2O+CO2↑;加热煮沸;(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)CaCO3+H2O+CO2═Ca(HCO3)2.

 中考解读考点精练系列答案
中考解读考点精练系列答案