
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
【答案】(1)样品中氧化铁的质量是20g -4 g= 16 g ……………………………… 1分
样品中,氧化铁的质量分数为 ×100%= 80%…………………… 1分
×100%= 80%…………………… 1分
(2)解:设所得溶液中溶质的质量为x。
Fe2 O3 + 6HCl===2 FeCl3 + 3H2O ……………………………………… 1分
160 325
16g X
 160 325
160 325
16g X
X == 32.5g …………………………………………………… 1分
所得溶液的质量为:184 g + 20 g - 4 g=200 g …………………………… 1分
所得溶液中溶质的质量分数为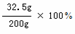 =16.25% …………………………1分
=16.25% …………………………1分
答:略。(单位和百分号都不在扣分范围内)
【解析】(1)由题意可知,剩余的4g固体为矿石中杂质的质量,则可知20g赤铁矿石中含氧化铁的质量为20g-4g=16g,赤铁矿中氧化铁的质量分数= ×100%= 80%。
×100%= 80%。
(2)由发生的反应可知,反应后所得溶液为生成的氯化铁的溶液,即本题要求反应后所得的氯化铁溶液的溶质质量分数。要想求解本题,需知道反应后溶液的质量和溶液中的溶质FeCl3的质量。溶液质量可根据质量守恒定律求得,即所得溶液质量为参加反应的氧化铁的质量与加入的稀盐酸的质量之和:20g-4g+184g=200g。而FeCl3的质量需根据化学方程式计算进行求解,计算时的已知量是参加反应的氧化铁的质量,设生成的氯化铁质量为x,据此根据化学方程式中各物质的质量比关系,列出比例式并求出x,最后根据溶质质量分数计算公式解答本题。


 优等生题库系列答案
优等生题库系列答案科目:初中化学 来源: 题型:
工业上采用离子交换膜电解槽电解饱和食盐水,可以得到高浓度的烧碱溶液(含NaOH35%~48%)。某学习小组为了验证附近氯碱化工厂产生的NaOH溶液是否达到高浓度标准,进行了如下操作,请你参与计算:
(1)到工厂采集了电解槽中的NaOH溶液100g。NaOH中氧元素的质量分数是 。
(2)在实验室用如右图所示浓硫酸配制200g24.5%的稀硫酸,计算所取浓硫酸的体积 (计算结果取整数)。

(3)进行中和测定,向采集到的溶液中逐滴加入所配制的稀硫酸,并不断测定溶液的pH值,当pH=7时,消耗稀硫酸160g。通过计算判断此时电解槽中NaOH溶液是否达到高浓度标准。
查看答案和解析>>
科目:初中化学 来源: 题型:
某厂排放的废水中含有碳酸钠,未经处理,会造成污染.化学兴趣小组的同学对废水处理设计了如图所示的实验方案.

试计算:
(1)反应生成CO2气体的质量是 2.2 g.
(2)反应后所得溶液中溶质的质量分数?
(温馨提示:Na2CO3+2HC1═2NaC1+H2O+CO2↑)
查看答案和解析>>
科目:初中化学 来源: 题型:
重铬酸钾(K2Cr2O7,Mr=294。铬元素为+6价,Mr表示相对分子质量)是一种重要的化工原料,在皮革工业、有机反应中都有广泛应用。但+6价铬有很强的毒性易污染环境,使用后,须用绿矾(FeSO4·7H2O,Mr=278)将其变成低毒性+3价铬才能做后续处理.
反应原理:6FeSO4·7H2O+ K2Cr2O7+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+49H2O
现有1.0吨重铬酸钾需要处理,计算需要绿矾多少吨?(写出计算过程,结果精确小数点后1位)
查看答案和解析>>
科目:初中化学 来源: 题型:
常温下,氨气为无色有刺激性恶臭气味的气体,密度比空气小,易溶于水。氨气溶于水显弱碱性,实验室可用氯化铵固体和氢氧化钙固体混合加热制取。则下列说法正确的是( )
A.可用向下排空气法收集到氨气 B.氨水能使紫色石蕊试液变红色
C.多余的氨气可排放到大气中 D.实验室制氨气的发生装置与双氧水制氧气相同
查看答案和解析>>
科目:初中化学 来源: 题型:
(1)请用化学用语表示或写出符号的意义:
①氢氧根离子________;②二氧化硫中硫元素的化合价________;
③3H2O________。
(2)下列食物:①米饭;②鸡蛋;③大豆油;④西红柿。能提供大量蛋白质的是__________(填序号),蛋白质属于______(填“无机物”或“有机物”)。
(3)香烟烟雾中含有多种有害物质,毒副作用大的有________、尼古丁和焦油,不吸烟的人能闻到烟味的原因是________;随手丢弃的烟头还容易引发火灾,原因是(填字母)________(A.提供可燃物 B.提供氧气 C.使可燃物的温度达到着火点)。一旦发生火灾,消防队员通常用水来灭火,该方法的化学原理是
______________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如表:
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 4.2 | 2 | 0 | 9.2 |
下列说法正确的是( )
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20℃时四种物质溶解度的关系为:丙>乙>甲>丁
D.四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com