
经测定,甲醛(CH2O)、醋酸(C2H4O2)、丙酮(C3H6O)三种物质的混合物中含氢元素8g,则该混合物完全燃烧后产生二氧化碳气体的质量是
A.48g B.72g C.120g D.176g
D
【解析】
试题分析:由甲醛、醋酸和丙酮的化学式可知,每个分子中的C、H原子个数比均为1:2,则C、H元素质量比均等于(1×12):(2×1)=6:1;根据题意,混合物中含氢元素8g,则混合物中含碳元素的质量为8g×6=48g;根据质量守恒定律可知,混合物中所含有的碳元素的质量=完全燃烧后产生的二氧化碳气体中碳元素的质量。再结合“物质的质量=物质中某元素的质量÷该元素的质量分数”可知,燃烧后产生的二氧化碳气体的质量=48g÷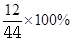 =176g。故选D
=176g。故选D
考点:元素质量比的计算,化合物中某元素的质量计算,质量守恒定律及其应用
点评:本题主要考查有关化学式的计算,熟练掌握相关计算的方法,是解题的关键,此外还应注意元素守恒思想在解题中的重要作用。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?湘潭)据报道,山东一些不法蔬菜商贩使用甲醛溶液喷洒白菜进行保鲜.甲醛(HCHO)是一种无色有强烈刺激性气味的气体,易溶于水,能在氧气中完全燃烧生成二氧化碳和水,是重要的工业生产原料,有毒,被世界卫生组织确定为致癌和致畸形物质.
(2012?湘潭)据报道,山东一些不法蔬菜商贩使用甲醛溶液喷洒白菜进行保鲜.甲醛(HCHO)是一种无色有强烈刺激性气味的气体,易溶于水,能在氧气中完全燃烧生成二氧化碳和水,是重要的工业生产原料,有毒,被世界卫生组织确定为致癌和致畸形物质.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2013年江苏省扬州中学树人学校中考化学一模试卷(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源: 题型:
经测定,甲醛(CH2O)、醋酸(C2H4O2)、丙酮(C3H6O)三种物质的混合物中 含氢元素8g,则该混合物完全燃烧后产生二氧化碳气体的质量是
含氢元素8g,则该混合物完全燃烧后产生二氧化碳气体的质量是
A. 48g B. 72g C.120g D.176g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com