
�ڴ����������£���O2��HClת��ΪCl2�������Ч�棬������Ⱦ����Ҫ��������ͼ�����й��ڸ�ԭ��˵������ȷ����

A. ��Ӧ�����л��ϼ۸ı��Ԫ����Cl��O��Cu
B. �漰�ķ�Ӧ�����и��ֽⷴӦ���û���Ӧ
C. �����ϣ�ÿ����71gCl2������Ҫ����73gHCl
D. �����ϣ�ÿ����73gHCl����������ϵ���ٲ���80gCuO
AD ����������������ͼ��֪����ӦI�У�����ͭ��ϡ���ᷴӦ�����Ȼ�ͭ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��2HCl+CuO�TCuCl2+H2O����Ӧ���У�����ͭ��ϡ���ᷴӦ�����Ȼ�ͭ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��O2+ CuCl2�TCuO +Cl2��A����Ӧ���������Ԫ�صĻ��ϼ���-1�۱�Ϊ0����Ԫ�صĻ��ϼ���0�۱�Ϊ-2��Cu�Ļ��ϼ�ʼ��Ϊ-2��û�иı䣬����B�� ��ӦI�����ֻ�����������ɷ���������... ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ʡ2018����꼶��ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ� ���ͣ������
��ͼ�ֱ��Ǽ�Ԫ�ء���Ԫ�ء���Ԫ�ء���Ԫ�ص�ԭ�ӽṹʾ��ͼ

��1��A��X��ֵΪ________��
��2��A��D��ѧ�������Ƶ�ԭ����_____________��
��3����ͼ��Ԫ�ء���Ԫ�ص��������ֱ�Ϊ8��1����һ��OH- �����������ӣ���������Ϊ_________��
��4��AC�γɵ����ʵĻ�ѧʽΪ______________��
19 ������������� 9 K2O ����������1����Aͼ��һ�ֽṹʾ��ͼ����X=2+8+8+1=19�� ��2����AD�������ĵ���������1���ʻ�ѧ�������ƣ� ��3��������ĵ��ӿ��Ե�ʧ���������Ӳ��ܵ�ʧ�������������ӵ�������Ϊ1+8=9�� ��4��Aԭ�ӵ�������������1���ڻ���������+1�ۣ�Cԭ�ӵ�������������6 ���ڻ���������-2�ۣ����γɵĻ�ѧʽ��K2O�� ...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2018����꼶��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��ͼ��ʾ��A��B��C�������ʵ��ܽ�����ߣ��ݴ�ͼ�ش�

��1��t1��ʱ��A��B��C�������ʵ��ܽ���ɴ�С��˳���� ��
��2��t2��ʱ����30gA����100gˮ�У���ֽ������������Һ���������������� ��
��3��t3��ʱ����������A��B�������ʵı�����Һ���µ�t2��ʱ���������������ϴ���� ��
��4��t3��ʱ����25gC����100gˮ�У���ֽ����õ�C�ı�����Һ���ڲ��ı��ܼ�����ǰ���£������Ϊ��������Һ�ķ����� ��
��1��C��B��A����2��20%����3��A����4������������t2�� �������� �����������1��t1��ʱ��A��B��C�������ʵ��ܽ���ɴ�С��˳���ǣ�C��B��A�� ��2��t2��ʱ��A���ܽ����25g�����Խ�30gA����100gˮ�У���ֽ������ȫ���ܽ⣬����ܽ�25g����������Һ���������������ǣ���100%=20%�� ��3��t3�桫t2�棬A���ܽ�ȱ仯���ȱ�B�����Խ���...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2018����꼶��ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ���ѡ��
�����ڼ���̳���˿ͺܶ࣬���˻�о�������ȱ�����ⶨ��������������������ǣ� ��
A. 1% B. 19% C. 25% D. 78%
B ����������������������Ŀ���������Լռ���������21%���̳���˿ͺܶ࣬���˻�о�������ȱ���������ĺ���Ӧ�Ե���21%���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����н�����2018����꼶��ѧ��һģ���Ի�ѧ�Ծ� ���ͣ�������
���ð���ʯ�Ʊ���ʽ̼��þ[4MgCO3��Mg(OH)2��4H2O]���������¡�

(1)����ʯ��Ҫ����MgCO3��CaCO3��������ʯ��ʯ�������ú�ۻ�ϣ��ڻ�����Ҥ�г����������MgO��CaO�������м���ú��������____________________��ˮ��ʱ����Ҫ��ӦΪMgO+H2O=Mg(OH)2��______________(�ѧ����ʽ)��
(2)̼����������Һ��pH���ϼ�С��Ϊʵ��þԪ�����Ԫ�صķ��룬�������Һ��pH��8.5��9֮�䣬ʹ��Mg(OH)2ת��Ϊ���ܵ�Mg(HCO3)2��pH=9����Һ����_______(����ԡ������ԡ������ԡ�)��ʵ������pH��ֽ�ⶨ��ҺpH�ķ�����_______��
(3)����Ʒ����Ҫ�ɷ���_________������X��________���Ƚ�ʱ�Ȳ���MgCO3��3H2O������MgCO3��3H2O�ٷֽ�����4MgCO3��Mg(OH)2��4H2O����MgCO3��3H2O�ֽⲻ��ȫ�����Ʒ��þԪ�ص���������__________��(�ƫ�����䡱��ƫС��)
(4)����ʱ��������CO2����ֱ�ӹ���̼���⣬���ɽ�CO2ת��Ϊ���ֻ�����Ʒ��
�ٹ�ҵ�����÷�Ӧ��CO2 + H2 HCOOH���������ᡣ��Ӧ�е�����������ͬ���¶ȡ�CO2��ʼѹ���Դ����Ĵ�����Ӱ��ֱ�����ͼ��ʾ������ѵķ�Ӧ�¶�Ϊ__________�棬��ѵ�CO2ѹ��Ϊ_________MPa��
HCOOH���������ᡣ��Ӧ�е�����������ͬ���¶ȡ�CO2��ʼѹ���Դ����Ĵ�����Ӱ��ֱ�����ͼ��ʾ������ѵķ�Ӧ�¶�Ϊ__________�棬��ѵ�CO2ѹ��Ϊ_________MPa��


��CO2�ͼ��鷴Ӧ���ƺϳ���(CO��H2�Ļ����)����Ч����CO2����һ�ַ������ڴ�����800�������£�CO2��CH4��һ��������Ӧ��������ȫת��Ϊ�ϳ������仯ѧ����ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����н�����2018����꼶��ѧ��һģ���Ի�ѧ�Ծ� ���ͣ���ѡ��
�����ˮ��Ӧ������ˮú�����䷴Ӧ����ʾ��ͼ��ͼ��ʾ��
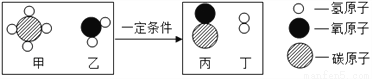
���жԸ÷�Ӧ��������ȷ����
A. ��Ӧǰ��ԭ������ı� B. ��Ӧǰ�������Ŀ����
C. ��Ӧ��û��Ԫ�ػ��ϼ۵ĸı� D. �÷�Ӧ�У����Ͷ���������Ϊ14��3
D ������������ʾ��ͼ��֪���÷�Ӧ�ķ�Ӧ���Ǽ����ˮ����������һ����̼����������Ӧ�Ļ�ѧ����ʽΪ��CH4+H2O CO+3H2��A������ʾ��ͼ�����ı仯��֪����Ӧǰ��ԭ�ӵ�����䣬����B���ɷ�Ӧ�Ļ�ѧ����ʽ��֪��ÿ2�����ӱ仯����4�����ӣ���Ӧǰ�������Ŀ�����˱仯������C����Ӧǰ����Ԫ�صĻ��ϼ���+1����Ӧ����0����Ӧǰ����Ԫ�صĻ��ϼ۷����ı䣬����D������������ʽ��֪���÷�...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����н�����2018����꼶��ѧ��һģ���Ի�ѧ�Ծ� ���ͣ���ѡ��
��Ӧ2NH4ClO4 ==== N2��+Cl2��+2O2��+4X��X�Ļ�ѧʽ��
A. H2 B. H2O C. H2O2 D. HCl
B ���������������غ㶨�ɣ���Ӧǰ��ԭ�����ࡢ��Ŀ�����䣬�ɷ�Ӧ�Ļ�ѧ����ʽ2NH4ClO4 ==== N2��+Cl2��+2O2��+4X����Ӧǰ�����⡢�ȡ���ԭ�Ӹ����ֱ�Ϊ2��8��2��8����Ӧ����������е����⡢�ȡ���ԭ�Ӹ����ֱ�Ϊ2��0��2��4�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��4X�����к���8����ԭ�Ӻ�4����ԭ�ӣ���ÿ��X������2����ԭ�Ӻ�1����ԭ�ӹ��ɣ�����X�Ļ�ѧʽΪH2O����ѡB...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ������2018�������ѧģ����Ծ�(5) ���ͣ���ѡ��
��ͼװ�ÿ�����������ռ������顢���Ӻ�����IJ����ȣ�������ɵ�ʵ����

A. �����a��ͨ�룬�ռ�����
B. ƿ��װ�г���ʯ��ˮ�������������Ƿ���ж�����̼
C. ƿ��װ������������Һ������һ����̼�л��еĶ�����̼
D. ��b�˽���Ͳ��ƿ��װ��ˮ��������������
D �����������������A�������a��ͨ�룬�ռ���������A����B��ƿ��װ�г���ʯ��ˮ�������������Ƿ���ж�����̼����B��ȷ��C��ƿ��װ������������Һ������һ����̼�л��еĶ�����̼����C��ȷ��D����a�˽���Ͳ��ƿ��װ��ˮ������������������D��ȷ�� ����ÿ���������ռ������顢���Ӻ�����IJ�����֪ʶ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ�����г�����2018����꼶��һ��ģ�⿼�Ի�ѧ�Ծ� ���ͣ��ۺ���
Ϊ�˲ⶨij������Ʒ(����Ϊ�Ȼ���)��̼���Ƶ�����������С��ͬѧ����Ʒ����������ͼ����ʵ��:
ʵʼ���� | �ٳ�ȡ�ձ������� | �ڽ�������������ձ��в����� | �۳�ȡ����������Ʒ�����ձ��У�ʹ֮�����ϡ���ᷴӦ | �ܴ���Ӧ��ȫ���� |
ʵ��ͼʾ |
| |||
ʵ������ | �ձ�������Ϊ50.0 | �ձ������������Ϊ��100.0 | ��Ʒ������11.0g | �ձ������л���������106.6g |
��1�������ˮ��Һ��__________(����ԡ��������ԡ������ԡ�֮һ)
��2����ʵ�������ɶ�����̼������Ϊ___________;
��3��ͨ����ѧ����ʽ������Ʒ��̼���Ƶ���������(��������ȷ��0.1g)______;
���� 4.4�� 96.4% ��������(1) ��1�������ˮ��Һ�Լ��ԣ���2�����������غ㶨�ɵã���Ӧ�ų�CO2������=(100.0g+11.0g)?106.6g=4.4g�� (2)��11.0g̼������Ʒ�к�Na2CO3����Ϊx Na2CO3+2HCl�TNaCl+CO2��+H2O 106 44 x 4.4g ...�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com