



科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
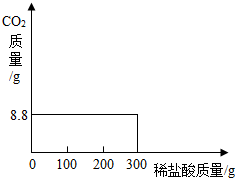 (2003?扬州)在我国青海湖地区有一种说法:冬天捞碱,夏天晒盐.这里的碱是指Na2CO3,盐是指NaCl.人们从盐湖中捞得的Na2CO3会含有少量的NaCl.
(2003?扬州)在我国青海湖地区有一种说法:冬天捞碱,夏天晒盐.这里的碱是指Na2CO3,盐是指NaCl.人们从盐湖中捞得的Na2CO3会含有少量的NaCl.| 实验次序 | 每次产生的CO2的质量(g) |
| 第一次先逐滴加盐酸100g | 0 0 |
| 第二次再逐滴加盐酸100g | 8.8 |
| 第三次再逐滴加盐酸100g | 0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2008?静安区二模)A、B两种固体物质的溶解度曲线如图所示.请回答:
(2008?静安区二模)A、B两种固体物质的溶解度曲线如图所示.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com