
甲、乙两溶液中分别含有以下六种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 中的三种和两种,且甲、乙两溶液中均无沉淀物.若将甲、乙溶液以适当比例混合,则可生成四种沉淀物且其中三种是氢氧化物,过滤后,排放出的是同一种钠盐的稀溶液.试推断:
中的三种和两种,且甲、乙两溶液中均无沉淀物.若将甲、乙溶液以适当比例混合,则可生成四种沉淀物且其中三种是氢氧化物,过滤后,排放出的是同一种钠盐的稀溶液.试推断:
①甲溶液中含有________,________,________.
②乙溶液中含有________,________.
③写出生成氢氧化物沉淀的有关反应的化学方程式:
________________________________________________________.
________________________________________________________.
________________________________________________________.
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
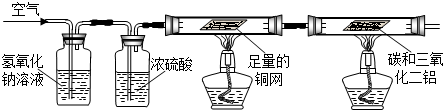
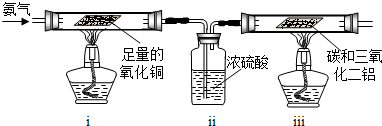
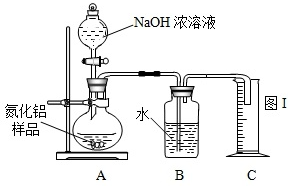
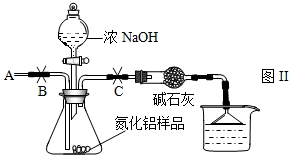
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com