【答案】
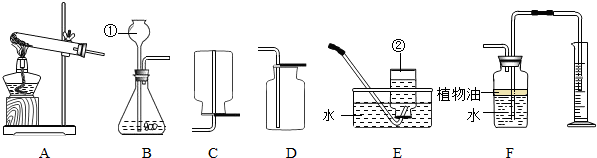
分析:(1)熟悉常见仪器的名称和用途;
(2)根据实验室用高锰酸钾制取氧气的原理、步骤及注意事项进行分析,写出反应的方程式;
(3)根据氢气和空气的密度的关系进行分析;
(4)根据二氧化碳的溶解性进行分析;
(5)对比装置C、B,分析在控制反应进行操作上简便性;
(6)①根据表中的数据分析浓度对反应速率的影响;
②根据表中的数据分析温度对反应速率的影响;
③根据防止硫酸钙覆盖在大理石上分析应进行的操作;
④根据药品的接触面积对反应的影响分析.
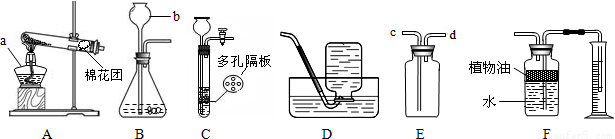
解答:解:(1)标号仪器的名称是a酒精灯,b长颈漏斗;
(2)实验室用高锰酸钾制取氧气的属于加热固体制取气体,应选用装置A.,由于氧气的密度大于空气、不易溶于水,所以收集装置可选用装置D或E,反应的方程式是:2KMnO
4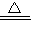
K
2MnO
4+MnO
2+O
2↑,该反应由一种物质生成了三种物质属于分解反应,用排水法收集氧气时,氧气集满的实验现象是:有气泡从集气瓶口往外冒出;
(3)由于氢气的密度小于空气的密度,所以用E装置收集氢气,则氢气应从d 口通入;
(4)由于二氧化碳能溶于水,所以其中在水面上放一层植物油的目的是防止二氧化碳溶于水;
(5)装置C相对于装置B在操作方面的优势为:随开随用,随关随停;
(6)①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为25%,因为浓度小于或大于此浓度对反应的影响是 生成气体体积较少;
②在合适的硫酸浓度下,应选择最合适的反应温度为70℃;
③为防止硫酸钙覆盖在大理石上,应增加振荡 操作,更有利于气体的制备;
④通过反应的速率可以看出,该研究小组为了研究固液接触面积 对该反应速率的影响,在28℃进行了如下实验.
故答为:
(1)酒精灯,长颈漏斗;
(2)A,D或E,2KMnO
4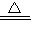
K
2MnO
4+MnO
2+O
2↑,分解,防止高锰酸钾粉末堵塞导管影响气体导出,有气泡从集气瓶口往外冒出;
(3)d;
(4)防止二氧化碳溶于水;
(5)随开随用,随关随停;
(6)①25%,生成气体体积较少;②70; ③振荡;④固液接触面积.
点评:熟练掌握实验室中制取气体的发生装置和收集装置的选择依据,并能作出正确的选择,记住常见气体制取的反应原理,并能够正确书写化学方程式.

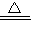 K2MnO4+MnO2+O2↑,该反应由一种物质生成了三种物质属于分解反应,用排水法收集氧气时,氧气集满的实验现象是:有气泡从集气瓶口往外冒出;
K2MnO4+MnO2+O2↑,该反应由一种物质生成了三种物质属于分解反应,用排水法收集氧气时,氧气集满的实验现象是:有气泡从集气瓶口往外冒出;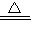 K2MnO4+MnO2+O2↑,分解,防止高锰酸钾粉末堵塞导管影响气体导出,有气泡从集气瓶口往外冒出;
K2MnO4+MnO2+O2↑,分解,防止高锰酸钾粉末堵塞导管影响气体导出,有气泡从集气瓶口往外冒出;

 阅读快车系列答案
阅读快车系列答案