
 有3g混有碳酸钠的氯化钠固体样品,向其中滴加盐酸,加入盐酸的质量与生成二氧化碳气体的质量符合右图所示的质量关系.(不计损耗)
有3g混有碳酸钠的氯化钠固体样品,向其中滴加盐酸,加入盐酸的质量与生成二氧化碳气体的质量符合右图所示的质量关系.(不计损耗)| 106 |
| 44 |
| x |
| 0.44g |
| 1.94g |
| 3g |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
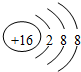 ,则下列说法不正确的是( )
,则下列说法不正确的是( )| A、该元素是一种非金属元素 |
| B、该微粒是带两个单位负电荷的阴离子 |
| C、该微粒的质子数是18 |
| D、该微粒的原子核外有18个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、+l | B、+2 | C、+3 | D、+4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、铁丝分别放入硝酸铜溶液和硝酸银溶液 |
| B、铁丝放入硝酸铜溶液,铜丝放入硝酸银溶液 |
| C、铜丝放入硝酸亚铁溶液,铁丝放入硝酸银溶液 |
| D、银丝分别放入硝酸铜溶液和硝酸亚铁溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:

| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中, 滴加氢氧化钙溶液 | 猜想②正确 相关的化学方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 选 项 | 物 质 | 所含杂质 | 除去杂质的办法 |
| A | N2 | O2 | 通过足量的灼热铜网 |
| B | CO2 | CO | 通过足量的灼热氧化铜 |
| C | H2 | 水蒸气 | 通过盛有氧化钙固体的干燥管 |
| D | CO2 | HCl | 通过盛有足量氢氧化钠溶液的洗气瓶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com